| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ�ر�֪ʶ�㡶ԭ���ԭ������Ƶ����̣�2017�����°棩(��)
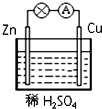 �ο��𰸣�ͼΪͭпԭ��أ�Zn��Cu���ã�ӦΪԭ��صĸ�����������ӦΪZn-2e-�TZn2+�� ��������� �����Ѷȣ�һ�� 3������� ������Ԫ�����ڱ���һ���֣�����Ԫ�آ٣����ڱ��е�λ�ã����û�ѧ����ش��������⣺
��1���ܡ��ݡ���ԭ�Ӱ뾶�ɴ�С��˳��Ϊ(Ԫ�ط���)________________________�� ��2���ڡ��ۡ��ߵ���ۺ������������ǿ������˳����(�ѧʽ)________ �� ��3���١��ܡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ����д������һ�ֻ�����Ļ�ѧʽ��_______________�� ��4���ɢں͢���ɵĻ�������ݵ�ͬ������������Ԫ�صĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ:_______�� ��5��������ݵ�����������ˮ���ﷴӦ�����ӷ���ʽΪ �� ��6�����â٢��������л�����Ϊȼ�ϵ�ص�ԭ�ϣ���д���ڼ��Խ�����ȼ�ϵ�ظ����ĵ缫��Ӧʽ: �� ��7��ȼú�����еĺ��е������NOx����������̼�����壬�������з�����ȼú����������������ʱ�������ü������ԭ������� �磺CH4(g)��4NO2(g)=4NO(g)��CO2(g)��2H2O(g) �� ��H=��574 kJ��mol��1 CH4(g)��4NO(g)=2N2(g)��CO2(g)��2H2O(g) �� ��H=��1160 kJ��mol��1 ��CH4(g)��NO2(g)��ԭΪN2(g)�ȵ��Ȼ�ѧ����ʽΪ �� �ο��𰸣���1��Na��Al��O������2�֣� �������������Ԫ�������ڱ��е�λ�ÿ�֪����ΪH����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪSi����ΪCl���� �����Ѷȣ����� 4��ѡ���� �����ʺϵ�����������Ӧ2Fe3++2I- �ο��𰸣�C ��������� �����Ѷȣ�һ�� 5��ѡ���� ����װ���е���������ͨ�����ǣ������� �ο��𰸣�A��B��C�����γ��Է���������ԭ��Ӧ�����γ�ԭ��ط�Ӧ�������е���ͨ����D�в����γɱպϻ�·�������γ��Է���������ԭ��Ӧ�������γ�ԭ��ط�Ӧ�� ��������� �����Ѷȣ��� | |||||||||||||||||||||||||||||||||||||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ����ɡ������Ǻ�.. | |
| �����Ŀ |