1、选择题 某密闭容器中发生如下反应:2X(g)+Y(g)  ?Z(g);△H <0?下图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是
?Z(g);△H <0?下图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是
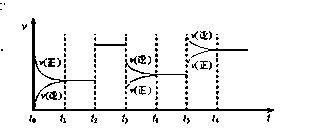
A.t3时减小了压强
B.t5时增大了压强
C.t6时刻后反应物的转化率最高
D.t1 - t2时该反应的平衡常数大于t6 时反应的平衡常数
参考答案:BC
本题解析:A、减小压强,平衡向增大体积的方向移动,所以一开始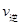 >
> ,随后又逐渐恢复到原来的反应速率,错误;B、增大压强,平衡向减少体积的方向移动,一开始
,随后又逐渐恢复到原来的反应速率,错误;B、增大压强,平衡向减少体积的方向移动,一开始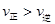 ,随后又逐渐恢复到原来的反应速率,正确;C、当不改变反应物用量,平衡向你反应方向移动,反应物的转化率降低,正确;D、根据平衡常数的公式,错误。
,随后又逐渐恢复到原来的反应速率,正确;C、当不改变反应物用量,平衡向你反应方向移动,反应物的转化率降低,正确;D、根据平衡常数的公式,错误。
本题难度:一般
2、选择题 相同温度下,两个恒压且压强相同的密闭容器中发生可逆反应
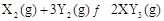 ?
?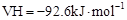
实验测得反应在起始及达到平衡时的有关数据如下表所示:
容器编号
| 起始时各物质物质的量/mol
| 达平衡时体系能量变化
|
X2
| Y2
| XY3
|
①
| 0.1
| 0.3
| 0
| 4.63 kJ
|
②
| 0.8
| 2.4
| 0.4
| Q(Q>O)kJ
|
下列叙述正确的是(?)
A.反应的平衡常数:①>②
B.达平衡时,两个容器中XY3的物质的量浓度均为
C.若容器①体积为0.20L.则达平衡时放出的热量大于4.63kJ
D.达到平衡时,容器①、②中各物质的百分含量相同
参考答案:D
本题解析:平衡常数只与温度有关系,A不正确;根据①中放出的热量可知,生成物XY3的物质的量是4.63 kJ÷92.6kJ/mol×2=0.1mol容器容积不能确定,所以不能计算浓度,B不正确;放出的热量与容器容积无关系,C不正确;由于压强和温度相同,且X和Y的物质的量之比是相同的,因此两容器中的平衡是等效的,D正确,答案选D。
本题难度:一般
3、填空题 某温度时,在2L容器中,X、 Y、Z三种物质的物质的量随时间变化的曲线如图所示,该反应的化学方程式为____,反应开始至2 min,用Z表示的平均反应速率为____。
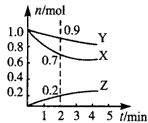
参考答案:3X+Y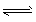 2Z? ;0.05 mol・L-1・min-1
2Z? ;0.05 mol・L-1・min-1
本题解析:
本题难度:一般
4、选择题 N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)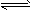 4NO2(g)+ O2(g) △H >0 T1温度下的部分实验数据为
4NO2(g)+ O2(g) △H >0 T1温度下的部分实验数据为
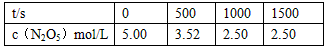
下列说法不正确的是
[? ]
A.500s内N2O5分解速率为2.96×10-3 mol/(L・s)
B.T1温度下的平衡常数为K1=125,1000s时转化率为50%
C.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2
D.T1温度下的平衡常数为K1 ,T3温度下的平衡常数为K3,若K1> K3,则T1 >T3
参考答案:C
本题解析:
本题难度:一般
5、选择题 已知 ,若反应速率分别用
,若反应速率分别用 .
.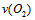 .
.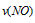 .
.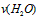 表示,则正确的关系式是
表示,则正确的关系式是
[? ]
A.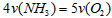
B.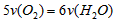
C.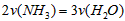
D.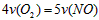
参考答案:D
本题解析:
本题难度:简单