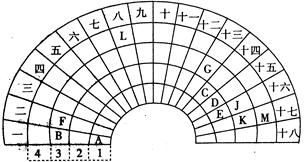
1、填空题 元素周期表的形式多种多样,下图是扇形元素周期表的一部分,对照中学化学常见长式元素周期表,回答下列问题:
(1)元素C的最高价氧化物的电子式为?;元素G的离子结构示意图为?。
(2)元素L位于周期表的第?族, 1mol/L LM2溶液500ml与0.4 mol K单质恰好完全反应的离子方程式为_______________________________________。
(3)化合物X是由B、E、G三种元素组成,其水溶液呈_______性,原因是___________
_____________________________________________________(用离子方程式表示)
(4)D和G组成的化合物GD,被大量用于制造电子元件。工业上用G的氧化物、C单质和D单质在高温下制备GD,其中G的氧化物和C单质的则该反应的化学方程式为?。
(5)制取粗硅的过程中,SiO是反应中间产物,隔绝空气时SiO和NaOH溶液反应(产物之一是硅酸钠)的化学方程式______________________________________________
参考答案:(1)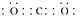 ?
?
(2)VIII? 10Fe2++6Br - +8Cl2=10Fe3++3Br2+16Cl-
(3)碱性,(1分) AlO2-+2H2O  Al(OH)3+OH-
Al(OH)3+OH-
(4)Al2O3+3C+N2  2AlN+3CO
2AlN+3CO
(5)? SiO+2NaOH=Na2SiO3+H2↑
本题解析:根据元素周期表中元素的相对位置,推A为氢、B为钠、C为碳、D为氮、E为氧、F为镁、G为铝、J为硫、K为氯、L为铁、M为溴。
(1)元素C的最高价氧化物为二氧化碳,电子式为 。元素G为铝,Al3+的离子结构示意图为
。元素G为铝,Al3+的离子结构示意图为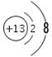 。
。
(1) ?
?
(2)元素L为铁,位于周期表的第VIII族? 1mol・L-1 LM2(FeBr2)溶液500mL与0.4 mol K单质(Cl2)的物质的量之比为5:4,恰好完全反应,因为还原性:Fe2+> Br-,因此Fe2+先被氧化:2Fe2++ Cl2 ?Fe3+ + 2Cl-,
?Fe3+ + 2Cl-,
每摩尔Fe2+反应用掉0.5molCl2,即按4:2反应,还剩余1.5mol的Cl2与Br-反应:2Br-+ Cl2 ?Br2 + 2Cl-,
?Br2 + 2Cl-,
注意只有3mol的Br-被Cl2氧化了,因为Cl2不足,整理得总反应:10Fe2+ +8Cl2+6Br- 10Fe3+ +16Cl- +3Br2。
10Fe3+ +16Cl- +3Br2。
(3)化合物X是NaAlO2,属于强碱弱酸盐, 水解显碱性,AlO2-+2H2O Al(OH)3+OH-。
Al(OH)3+OH-。
(4)化合物GD是AlN,G的氧化物是Al2O3,C单质是,D单质是氮气,Al2O3与C物质的量之比为1:3,用待定系数法。先假设Al2O3系数为1,C为3,可知AlN为2,N2为1,根据原子守恒,推知还生成3molCO,最后整理得Al2O3+3C+N2  2AlN+3CO。
2AlN+3CO。
(5)SiO和NaOH溶液反应,因为产物之一是酸钠,硅化合价由+2变为+4,化合价有升高,必然有化合价降低,分析可知,只有氢元素化合价可以降低,推出另一产物是氢气,配平得SiO+2NaOH=Na2SiO3+H2↑。
本题难度:一般
2、填空题 短周期元素A、B、C、D中,0.5 mol A元素的离子得到6.02×1023个电子后被还原为中性原子,0.4 克A的氧化物恰好与100 mL 0.2 mol・L-1的盐酸完全反应,A元素原子核内质子数与中子数相等;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请完成下列问题:
(1)推断A、B、C、D四种元素的符号:
A_______________;B_______________;C_______________;D_______________。
(2)C的原子结构示意图____________________________。
(3)D元素的最高价氧化物的结构式是________________。
(4)C、D元素组成的物质,分子内含有____________(填“极性”或“非极性”)键,其分子为______________(填“极性”或“非极性”)分子。
(5)用电子式表示A、C两元素形成化合物的过程:____________________________。
参考答案:(1)Mg? Al? Cl? C
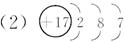
(3)O==C==O
(4)极性?非极性
(5)
本题解析:由0.5 mol A元素的离子得到6.02×1023个电子(1 mol e-)后被还原为中性原子,知A元素的化合价为+2;由AO+2HCl====ACl2+H2O,知0.4 g AO的物质的量n="0.2" mol・L-1×0.1 L÷2="0.01" mol,所以AO的摩尔质量为0.4 g/0.01 mol="40" g・mol-1;而A原子核内质子数与中子数相等,故A为Mg元素。B元素原子核外电子数比Mg原子核外电子数多1,所以B是Al元素。C-核外电子层数比Mg2+核外电子层数多1,则C是Cl元素。D元素原子最外层电子数是次外层的2倍,D是C元素。
本题难度:简单
3、选择题 硼的最高价含氧酸的化学式不可能是
A.H2BO4
B.H3BO3
C.HBO2
D.H2B4O7
参考答案:A
本题解析:硼为第二周期ⅢA族元素,最外层有3个电子,故在化合物中一般显示+3价,如B、C、D化合物;A中的B显示+6价。
点评:元素周期规律是高考必考知识点,考生在备考中应牢牢把握各规律的递变,并注意积累掌握短周期元素的结构与性质。
本题难度:一般
4、填空题 海水中富含氯元素。
(1)KCl广泛应用于医药和农业,KCl晶体中基态的氯离子电子排布式为?
(2)下列是部分金属元素的电离能
?
| X
| Y
| Z
|
第一电离能(KJ/mol)
| 520.2
| 495.8
| 418.8
|
已知X Y Z 的价层电子构型为nS1,则三种金属的氯化物(RCl)的熔点由高到低的顺序为?
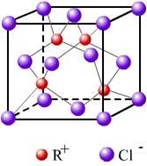
(3)RCl用作有机机合成催化剂, 并用于颜料, 防腐等工业。R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图所示。R的元素符号是?,与同一个Cl-相连的 R+有?个。
(4) 卤代烃在有机合成中作用巨大,烃基的结构对卤代烃的活性有很大的影响。CH3―CH2―Cl和碱溶液容易发生取代反应,而CH2=CH2―Cl 和碱溶液不起作用,请从结构上解释其差异?
(5) HCl和 HF结构相似,由于氢键的存在使两者性质上存在较大差异,请列举出由于氢键的影响导致的性质差异?
参考答案:(1)1s22s22p63s23p6 ?(2)ZCl<Ycl<XCl (3) Cu? 4?
(4)? CH3―CH2―Cl中与Cl原子成键的C以sp3杂化,而CH2=CH2―Cl中与Cl原子成键的C以sp2杂化,电子云密度不同;CH3―CH2―Cl中的C―Cl的键长比CH2=CH2―Cl中C―Cl要长;CH2=CH2―Cl的∏键对Cl的作用力比CH3―CH2―Cl的a键强。?
(5)HF沸点比HCl高;氢氟酸是弱酸,盐酸是强酸;实验测得HF分子质量偏大。
本题解析:本题考查物质结构与性质。主要考查点是电子排布式的书写、杂化轨道的基础知识、晶体的结构分析、电离能等。(2)已知X Y Z 的价层电子构型为nS1,说明三者在同一个主族,第一电离能逐渐减小,金属性逐渐增强,则原子半径逐渐增大,熔沸点逐渐减小;(3)R+中所有电子正好充满K、L、M 三个电子层,说明R的电子排布式为:1s22s22p63s23p63d10,是铜元素,从图中看出,一个R+有有4个Cl-相连,同理与同一个Cl-相连的 R+有4个;(4)CH3―CH2―Cl中与Cl原子成键的C以sp3杂化,而CH2=CH2―Cl中与Cl原子成键的C以sp2杂化,电子云密度不同;CH3―CH2―Cl中的C―Cl的键长比CH2=CH2―Cl中C―Cl要长;CH2=CH2―Cl的∏键对Cl的作用力比CH3―CH2―Cl的a键强;(5)氢键影响物质的物理性质。
本题难度:一般
5、选择题 在F、P、S三种元素中,每种元素都有某些方面区别于其他两种元素;若从中选出氟元素,选择的理由是(?)
A.单质与冷水反应非常剧烈
B.单质固态时属于分子晶体
C.一定条件下,能与氢气发生化合反应
D.最高价氧化物对应的水化物是强酸
参考答案:A
本题解析:略
本题难度:简单