?
参考答案:(14分)(1)Br2 + 2Fe2+  ?2Br-+ 2Fe3+(2分);? Br2(2分)。 ?2Br-+ 2Fe3+(2分);? Br2(2分)。
(2)乙(2分)?①否(2分)?② 2Fe3+ + 2I- ?I2 + 2Fe2+ (2分) ?I2 + 2Fe2+ (2分)
③请另外设计一个合理方案,证明已经发生反应。(以下每空2分)
实验操作
预期现象及结论
取少量黄色溶液,滴入几滴KSCN溶液
若溶液变红色,则证明已经发生反应
本题解析:略
本题难度:一般
2、选择题 研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是?
[?]
A.蒸馏常用于分离提纯液态有机混合物
B.燃烧法是研究确定有机物成分的有效方法
C.核磁共振氢普通常用于分析有机物的相对分子质量
D.对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团
参考答案:C
本题解析:
本题难度:简单
3、选择题 右图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与试验事实不相符的是
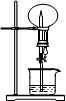
A.SO2 (NaOH溶液)无色喷泉
B.NH3(H2O含酚酞)红色喷泉
C.NO(H2O含石蕊)红色喷泉
D.HCl(AgNO3溶液)白色喷泉
参考答案:C
本题解析:SO2能被氢氧化钠溶液吸收,从而形成喷泉,A正确;氨气极易溶于水,且溶于水显碱性,B正确;NO不溶于水,不能形成喷泉,C不正确;氯化氢极易溶于水,且和硝酸银反应生成氯化银白色沉淀,D正确,答案选C。
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。该题的关键是明确喷泉实验的原理,以及气体溶于水的有关反应,然后结合题意灵活运用即可,有利于提升学生的学科素养。
本题难度:简单
4、实验题 (13分)某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】用葡萄糖制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag。
【设计实验方案,验证假设】
(1)甲同学从上述实验的生成物中检验出Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:?。甲同学还发现用同浓度FeCl3,Fe(NO3)3溶解银镜,FeC l3溶液溶解Ag的反应更快更完全,请解释其原因: l3溶液溶解Ag的反应更快更完全,请解释其原因:
(2)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
实验步骤(不要求写具体操作过程)
| 预期现象和结论
| ①
②
……
| 若银镜消失,假设2成立。
若银镜不消失,假设2不成立。
|
【思考与交流】
(3)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3-都氧化了Ag。
你是否同意丙同学的结论?,并简述理由:?。
参考答案:(1)Fe3++Ag= Fe2++Ag+(2分)? FeCl3中Cl-与Ag+生成AgCl,促进正向反应完全。(2分)
(2)①测定上述实验用的Fe(NO3)3溶液的pH;(2分)
本题解析:略
本题难度:简单
5、实验题 文献资料显示某地区的酸雨主要为硫酸型和盐酸型酸雨。某兴趣小组对酸雨进行实验研究:
(1) 提出合理的假设:该酸雨中的溶质除H2SO4、HCl外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有?。
(2) 设计实验方案验证以上假设。在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:盐酸、硝酸、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管。
实验步骤
| 预期现象和结论
| 步骤1:取适量酸雨于A、B两支洁净试管中,待用。
| ?
| 步骤2:往A试管中加入过量的Ba(OH)2溶液,静置,过滤。
| ?
| 步骤3:取少量步骤2得到的滤渣加入足量的盐酸。
| ?
| 步骤4:取少量步骤2得到的的滤液,加入?
?。
| ?
?
| 步骤5:往B试管中加入?
?。
| ?
?
参考答案:(12分)(1)SO2(或H2SO3)(2分)
(2)每空2分
实验步骤
预期现象和结论
步骤3:
若滤渣不完全溶解则酸雨中含有硫酸
步骤4:取少量步骤2得到的的滤液,加入过量的硝酸银,然后加入少量的硝酸银溶液
若产生白色沉淀,则酸雨中含有盐酸
步骤5:往B试管中加入几滴品红溶液,振荡
若品红溶液褪色,则所以中含有亚硫酸或SO2
本题解析:(1)由于酸雨中硫酸是亚硫酸被氧化后生成的,所以 主要溶质还一定有亚硫酸或SO2。
(2)由于硫酸钡和亚硫酸钡都是不溶于水的白色沉淀,但硫酸钡还不能溶于酸中,所以步骤3中,预期的现象和结论应该是:若滤渣不完全溶解则酸雨中含有硫酸;氯离子的检验一般用硝酸酸化的硝酸银溶液,所以步骤4应该是:取少量步骤2得到的的滤液,加入过量的硝酸银,然后加入少量的硝酸银溶液。预期的现象和结论应该是:若产生白色沉淀,则酸雨中含有盐酸。SO2的检验一般用品红溶液,所以步骤5应该是:往B试管中加入几滴品红溶液,振荡。预期的现象和结论应该是:若品红溶液褪色,则所以中含有亚硫酸或SO2。
点评:该题是高考中的常见考点,属于中等难度的试题。试题难易适中,侧重对学生基础性知识的巩固与训练,有助于培养学生综合实验能力和规范严谨的实验实际能力。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般
|
|