| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《pH计算》高频考点强化练习(2017年最新版)(二)
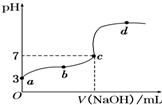 参考答案:A.由于甲酸中水电离的氢离子浓度很小,所以溶液中氢离子浓度与甲酸电离的甲酸根离子浓度基本相等,a点时溶液pH=3,氢离子浓度为10-3mol?L-1,则甲酸溶液中甲酸根离子浓度约为10-3mol?L-1,故A正确; 本题解析: 本题难度:一般 3、选择题 0.05mol/L的Ba(OH)2溶液,pH为( ) 参考答案:C 本题解析: 本题难度:一般 4、选择题 在一定体积的pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰 好完全沉淀时,溶液的pH=11。若反应后的溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则 参考答案:D 本题解析: 本题难度:一般 5、选择题 如图是向20.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH值变化的图象,根据图象分析,下列结论中不正确的是( ) |
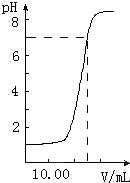
参考答案:C
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《物质的组成.. | |