1������� ��14�֣���1��NO2�н�ǿ�������ԣ��ܽ�SO2��������SO3����������ԭΪNO����֪��������Ӧ�����������仯��ͼ��ʾ��
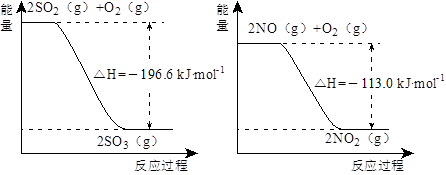
��NO2����SO2���Ȼ�ѧ����ʽΪ_________________________________��
��2����2L�ܱ������з���1mol��������һ���¶Ƚ������·�Ӧ��2NH3(g) N2��g��+3H2��g����
N2��g��+3H2��g����
��Ӧʱ��(t)��������������ѹǿ(p)�����ݼ��±�
ʱ��t/min
| 0
| 1
| 2
| 3
| 4
| 5
|
��ѹǿp
100 kPa
| 5
| 5.6
| 6.4
| 6.8
| 7
| 7
|
��ƽ��ʱ������ת����Ϊ___________��
��3��25�棬ij��Ԫ����H2A��NaOH��Һ��Ӧ������NaHA��Na2A����Һ�к�A�����ķֲ�������ƽ��ʱij��A����Ũ��ռ����A��Ũ��֮�͵ķ���������Һ�仯���������ͼ��ʾ��

��֪��103.04��1.1��103,104.37=2.3��104?25�棬Ka1(H2CO3)= 4.4��10-7 ?Ka2(H2CO3) �� 4.7��10-11
������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��c(A2-)/c(HA-)��ֵ?�����������С�����䡱����ͬ����c(H+)/c(OH-) ��ֵ?��
������0.1NaHAmol��L-1��Һ�м��백ˮ����Һ�����ԣ���c(H2A)+c(NH4+)?c(A2-) ������ڡ�����С�ڡ����ڡ�����
�ۼ���HA����������ƽ�ⳣ��Ka2=?��
��������H2A����Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ��?��
�ο��𰸣���1�� NO2(g)+SO2(g) SO3(g)+NO(g)? ��H=-41.8KJ/mol�� ��2��40%��
SO3(g)+NO(g)? ��H=-41.8KJ/mol�� ��2��40%��
��3������������ =����4.35��10-5����2H2A+CO32-=2HA-+CO2��+H2O
�����������1������ͼһ��֪�Ȼ�ѧ����ʽΪ��2SO2(g) +O2(g)  2SO3(g)��H="-196.6KJ/mol;" ��2NO(g)+ O2(g)
2SO3(g)��H="-196.6KJ/mol;" ��2NO(g)+ O2(g)  2NO2(g) ��H="-113.0KJ/mol;" �٣��������ɵ�NO2(g)+SO2(g)
2NO2(g) ��H="-113.0KJ/mol;" �٣��������ɵ�NO2(g)+SO2(g)  SO3(g)+NO(g)? ��H =��41.8KJ/mol����2�����ڷ�Ӧ��������̶��������н��У����Է�Ӧǰ���ѹǿ�ȵ�����������ʵ����ıȡ�2NH3(g)
SO3(g)+NO(g)? ��H =��41.8KJ/mol����2�����ڷ�Ӧ��������̶��������н��У����Է�Ӧǰ���ѹǿ�ȵ�����������ʵ����ıȡ�2NH3(g) N2��g��+3H2��g��������2xmol�İ�����Ӧ�������N2=xmol������H2=3xmol������δ��Ӧ�İ��������ʵ���Ϊ(1-2x)mol.n(ǰ)��n(��)=1����(1-2x)+x+3x��=1����1+2x��=5:7.���x=0.2.��������ת����Ϊ(2��0.2)��1��100%=40%;��3��?������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��������Ӧ��HA-+OH-=H2O+A2-������c(A2-)/c(HA-)��ֵ�������ϼ���NaOH��Һʱ��c(H+)��С��c(OH-) ��������c(H+)/c(OH-) ��ֵ��С���ڸ��������غ�ɵ�c(Na+)= c(HA-)+ c(H2A)+ c(A2-)�����ݵ���غ�ɵã�c(Na+)+ c(H+)+ c(NH4+)= c(OH-)+ 2c(A2-)+ c(HA-)������Ϊ��Һ�����ԣ�����c(H+)= c(OH-)��������ʽ�������ɵ�c(H2A)+c(NH4+)=c(A2-)����HA-
N2��g��+3H2��g��������2xmol�İ�����Ӧ�������N2=xmol������H2=3xmol������δ��Ӧ�İ��������ʵ���Ϊ(1-2x)mol.n(ǰ)��n(��)=1����(1-2x)+x+3x��=1����1+2x��=5:7.���x=0.2.��������ת����Ϊ(2��0.2)��1��100%=40%;��3��?������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��������Ӧ��HA-+OH-=H2O+A2-������c(A2-)/c(HA-)��ֵ�������ϼ���NaOH��Һʱ��c(H+)��С��c(OH-) ��������c(H+)/c(OH-) ��ֵ��С���ڸ��������غ�ɵ�c(Na+)= c(HA-)+ c(H2A)+ c(A2-)�����ݵ���غ�ɵã�c(Na+)+ c(H+)+ c(NH4+)= c(OH-)+ 2c(A2-)+ c(HA-)������Ϊ��Һ�����ԣ�����c(H+)= c(OH-)��������ʽ�������ɵ�c(H2A)+c(NH4+)=c(A2-)����HA- H++A2-����ͼ���֪�����ﵽ����ƽ��ʱc(HA-)=c(A2-).
H++A2-����ͼ���֪�����ﵽ����ƽ��ʱc(HA-)=c(A2-).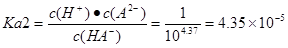 ��������H2A���������������ĵ���ƽ�ⳣ����֪������H2A���뵽Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ��2H2A+CO32-=2HA-+CO2��+H2O��
��������H2A���������������ĵ���ƽ�ⳣ����֪������H2A���뵽Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ��2H2A+CO32-=2HA-+CO2��+H2O��
�����Ѷȣ�һ��
2������� ��֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������ʾ��
��ѧʽ
| CH3COOH
| H2CO3
| HClO
|
����ƽ�ⳣ��
| Ka��1.8��10��5
| Kal��4.3��10��7
| Ka2��5.6��10��11
| Ka��3.0��10��8
|
| | | |
|
?
�ش��������⣺
��1�����ʵ���Ũ�Ⱦ�Ϊ0.1mol��L��1��������Һ��a��CH3COONa? b��Na2CO3?c��NaClO? d��NaHCO3
pH��С�������е�˳����_______________(�ñ����д)��
��2�������£�0.1mol��L��1CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�����?��
A��c(H�� )
B��c(H��)/c(CH3COOH)
C��c(H��)��c(OH��)
D��c(OH��)/c(H��)
E��c(H��)��c(CH3COO��)/c(CH3COOH)
��3�������Ϊ100mL pH��2��CH3COOH��һԪ��HX����ˮϡ������pH����Һ����Ĺ�ϵ����ͼ��ʾ����ͬ�¶�ʱHX�ĵ���ƽ�ⳣ��_?____(����ڡ�����С�ڡ����ڡ�)CH3COOH�ĵ���ƽ�ⳣ����������_____________________��

��4��25��ʱ��CH3COOH��CH3COONa�Ļ����Һ�������pH��6������Һ��c(CH3COO��)��c(Na��)��?mol��L��1(�ȷֵ)��
��5����״���£���1.12L CO2ͨ��100mL 0.75mol��L��1��NaOH��Һ�У�����Һ�����ӵ�Ũ���ɴ�С��˳��?
�ο��𰸣���1��a<d<c<b����1�֣�
��2��BD��2�֣�
��3�����ڣ�1�֣���ϡ����ͬ������һԪ��HX��pH�仯��CH3COOH�Ĵ�HX���Խ�ǿ������ƽ�ⳣ���ϴ�2�֣�
��4��9.9��10��7?��2�֣�
��5�� c(Na��)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)��2�֣�
�����������1��������Һ�У�ֻ��CH3COOH���ᣬ��ʾ���ԣ�ˮ��̶ȣ�CO32����ClO����HCO3����ˮ����Լ��ԣ�ˮ��̶�Խ����Խǿ�����Լ���˳���ǣ�Na2CO3��NaClO��NaHCO3����pH��С���������˳����CH3COOH��NaHCO3��NaClO��Na2CO3���ʴ�Ϊ��adcb����2��A��0.1mol?L��1��CH3COOH��Һ��ϡ�����У�����̶���������Ũ�ȼ�С����A����B��0.1mol?L��1��CH3COOH��Һ��ϡ�����У�������Ũ�ȼ�С��ͬʱ����ĵ��������ƶ���c��H+����С�ij̶�С��c��CH3COOH���ļ�С�̶ȣ�����c��H+��/c��CH3COOH������B��ȷ��C��Kw=c��H+��?c��OH����ֻ���¶ȵ�Ӱ�죬�¶Ȳ�������ֵ��һ����������C����D������ϡ�ͣ����Լ�����c��H+����С��������ǿ��c��OH��������c��OH����/c��H+������D��ȷ����ѡBD����3������CH3COOH��һԪ��HX��ˮϡ������pH����Һ����Ĺ�ϵͼ���Կ���HX����ϡ��������Һ��PH�仯�ȴ���Ĵ���������HXǿ�ڴ��ᣬ����̶ȣ�HX��CH3COOH���ʴ�Ϊ�����ڣ�ϡ����ͬ������һԪ��HX��pH�仯�ȴ��������ǿ������ƽ�ⳣ����4��CH3COOH��CH3COONa�Ļ����Һ�У����ڵ���غ㣺c��Na+��+c��H+��=c��OH����+c��CH3COO����������c��CH3COO������c��Na+��=c��H+����c��OH����=10��6mol/L��10��8mol/L=9.9��10��7mol/L����5����״���£���1.12L CO2��0.05mol,�� 0.075mol��NaOH��Ӧ������̼���ƺ�̼�����ƵĻ����Һ��������Ϊ0.025mol,��Һ�ʼ��ԣ�����̼�����ˮ������̼������ij̶Ƚϴ�����Һ�����ӵ�Ũ���ɴ�С��˳��c(Na��)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)��
�����Ѷȣ�����
3��ѡ���� ��֪��ͬ������ͬŨ�ȵ�NaCN��NaF��ϡ��Һ��ǰ�ߵ�pHֵ���ں��ߣ���ͬ�����±Ƚ�ͬŨ��ͬ���������Һ�еĹ�ϵ��������ȷ����
[? ]
A��c(CN-)>c(F-)
B��c(CN-)��c(F-) ?
C��NaCNˮ��̶ȱ�NaF��
D��NaCN����̶ȱ�NaF��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ����ѪҺ������pHԼΪ7.35��7.45�������������������ͻȻ�����ı�ͻ��������ж������ж���������������Σ�ա�����������Һ�Ļ���ϵͳ�д�������ƽ�⣺
H++HCO3�� H2CO3
H2CO3 CO2+H2O
CO2+H2O
H++PO43�� HPO42��?
HPO42��?
H++HPO42�� H2PO4��
H2PO4��
����ά��ѪҺpH������ȶ����Ա�֤���������������˵���в���������
A����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�
B����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�
C��ij�����ھ�����ע�Ĵ���������ˮ��ѪҺ��ϡ�ͣ��ᵼ��c(H+)�������٣�pHֵ���������ܻ�������ж�
D����������к����ʱ����CO2����ѪҺ����ʹƽ�������ƶ���c(H+)����pHֵ�Լ�С
�ο��𰸣�C
���������������Һ�Ļ���ϵͳ�д�������ƽ�⣺H++HCO3�� H2CO3
H2CO3 CO2+H2O��H++PO43��
CO2+H2O��H++PO43�� HPO42�� ��H++HPO42��
HPO42�� ��H++HPO42�� H2PO4�������Ե�ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�����A��ȷ����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�����B��ȷ��ij�����ھ�����ע�Ĵ���������ˮ��ѪҺ��ϡ�ͣ��ᵼ��c(H+)�������٣�����pHֵ�����С����C����Ϊ����Ĵ𰸣���������к����ʱ����CO2����ѪҺ����ʹƽ�������ƶ���c(H+)����pHֵ�Լ�С����D��ȷ��
H2PO4�������Ե�ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�����A��ȷ����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�����B��ȷ��ij�����ھ�����ע�Ĵ���������ˮ��ѪҺ��ϡ�ͣ��ᵼ��c(H+)�������٣�����pHֵ�����С����C����Ϊ����Ĵ𰸣���������к����ʱ����CO2����ѪҺ����ʹƽ�������ƶ���c(H+)����pHֵ�Լ�С����D��ȷ��
���������⿼���˵���ƽ�⣬��֪ʶ���Ǹ߿�������ص㣬�����ѶȲ���
�����Ѷȣ�һ��
5��ѡ���� �����£���amo1��L��1��ˮ����μ������ᣬ������������ȷ����
A����Һ��pH��С
B�� ����
����
C��ˮ�ĵ���̶��ȼ�С������
D�� ����
����
�ο��𰸣�C
���������A����ˮ�д��ڵ���ƽ��NH3��H2O NH4����OH�����������ᣬ��Һ��������ǿ��pH���ͣ�A��ȷ��B�������к������ӣ��ٽ�����ƽ��������Ӧ�����ƶ�����Һ��c(NH4��)����c(OH��)������
NH4����OH�����������ᣬ��Һ��������ǿ��pH���ͣ�A��ȷ��B�������к������ӣ��ٽ�����ƽ��������Ӧ�����ƶ�����Һ��c(NH4��)����c(OH��)������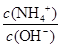 ����B��ȷ��C�����������ˮ�ĵ���ƽ�⣬������Һ��ˮ�ĵ���̶�ʼ���Ǽ�С�ģ�C����ȷ��D�����볣��ֻ���¶��й�ϵ������ˮ�ĵ��볣���Dz���ģ�D��ȷ����ѡC��
����B��ȷ��C�����������ˮ�ĵ���ƽ�⣬������Һ��ˮ�ĵ���̶�ʼ���Ǽ�С�ģ�C����ȷ��D�����볣��ֻ���¶��й�ϵ������ˮ�ĵ��볣���Dz���ģ�D��ȷ����ѡC��
�����Ѷȣ�һ��