1、选择题 下列表述中,合理的是
A.将水加热,Kw增大,pH不变
B.把FeCl3的水溶液加热蒸干可得到FeCl3固体
C.用25 mL碱式滴定管量取20.00mL高锰酸钾溶液
D.用惰性电极电解足量的Cu(NO3)2溶液时,当有0.2 mole-转移时会析出6.4g铜
参考答案:D
本题解析:电离是吸热的,所以将水加热,水的离子积常数增大,但pH减小,A不正确。氯化铁水解产生氢氧化铁和氯化氢,水解吸热,加热促进水解,同时氯化氢挥发,促使水解平衡进一步向正反应方向移动,所以最终得到的是氢氧化铁,B不正确。高锰酸钾溶液具有氧化性,能腐蚀橡胶,应该用酸式滴定管量取,C不正确。D中铜的化合价由+2价降低到0价,得到2个电子,所以D正确,答案选D。
本题难度:简单
2、填空题 工业上处理含有Cr2O72-的酸性工业废水,通常有两种处理方法。第一种方法是:先加入绿矾(FeSO4・7H2O),把废水中的Cr2O72-还原成Cr3+离子,再加入过量的石灰水,使Cr3+转变为Cr(OH)3沉淀。第二种方法是:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。试回答:
(1)电解时的电极反应:阳极?,阴极?。
(2)Cr2O72-转变成Cr3+的离子反应方程式:?。
(3)采用第二种方法时,往工业废水里加入适量的NaCl的目的是?。
(4)能否用石墨电极来代替Fe电极??(填“能”或“不能”),简述理由:
?。
参考答案:(1)Fe-2e-=Fe2+(1分) 2H++2e-=H2↑(1分)
(2)6Fe2++ Cr2O72-+14H+ = 6Fe3++2Cr3++7H2O(2分)
(3)增强溶液(或废水)的导电性。(1分)
(4)不能,因为阳极不能产生能将Cr2O72-还原到Cr3+的Fe2+。(2分)
解析:由于Cr(Ⅵ)的化合物毒性远高于Cr(Ⅲ)化合物,将Cr(Ⅵ)转化为Cr(Ⅲ),对废水进行处理是电化学知识在实际生活中的具体运用。在处理有关问题时,应注意思维的有序性:首先应考虑,溶液中阴阳离子在外电场作用下的定向迁移;然后再考虑阴阳两极按放电顺序可能发生的电极方程式。阴极:2H++2e-=H2↑,阳极:Fe-2e-=Fe2+,产生的Fe2+在向阴极迁移的过程中与向阳极迁移的Cr2O72-相遇,发生氧化还原反应:6Fe2++ Cr2O72-+14H+ = 6Fe3++2Cr3++7H2O,使Cr2O72-转化为Cr3+,同时Fe2+也转化为Fe3+。在以上电解的阴极反应及Fe2+与Cr2O72-的氧化还原反应中都消耗了大量的H+,溶液的pH不断变大,有利于Fe3+,Cr3+生成相应的Fe(OH)3、Cr(OH)3沉淀。若将Fe电极改成为石墨电极,由于不能产生的Fe2+,而不能将Cr2O72-转化为毒性较低的Cr3+,显然是不行的。
本题解析:略
本题难度:一般
3、选择题 化学与社会、生产、生活息息相关,以下对化学知识应用合理的是
①向奶粉中添加三聚氰胺,提高蛋白质的含量.给婴幼儿健康带来危害,因此我们应尽量少食用含有食品添加剂的食品,以防中毒
②超市不再提供免费塑料袋,可以帮助控制“白色污染”
③纯铁比普通钢更耐腐蚀,应多用纯铁作材料
④多位科学家因研制出新型催化剂而获得诺贝尔奖.是因为催化剂可以最大限度的提
高反应物的转化率( )
A.①②正确
B.只有②③正确
C.只有②正确
D.①②③④均正确
参考答案:①食品添加剂是指用于改善食品口味、延长食品保存期甚至增加食品营养成分的一类天然或化学合成物质,但如果被过度使用,则会危害人的健康,但不是中毒,故①错误;
②超市不再提供免费塑料袋,减少了塑料袋的使用,可以帮助控制“白色污染”,故②正确;
③纯铁比普通钢更耐腐蚀,但纯铁质软,所以纯铁不能作材料,故③错误;
④催化剂只能改变反应速率,不能改变反应的限度提高反应物的转化率,故④错误;
故选C.
本题解析:
本题难度:简单
4、选择题 下列方法不能防止铁管被腐蚀的是( )
A.与铜片相连
B.外表涂油漆
C.制成镍铬不锈钢合金
D.电镀
参考答案:A、和铜片相连时,金属铁为负极,更易腐蚀,故A正确;
B、铁生锈的主要条件是与空气和水(或水蒸气)直接接触,如果隔绝了空气和水,就能在一定程度上防止铁生锈,在钢铁表面涂油、刷漆都能防止钢铁生锈,故B错误;
C、铁生锈的主要条件是与空气和水(或水蒸气)直接接触,如果隔绝了空气和水,就能在一定程度上防止铁生锈,钢铁制造成耐腐蚀的合金能防止钢铁生锈,故C错误;
D、在金属铁的表面镀上一层比金属铁活泼的金属,可以防止铁被腐蚀,故D错误.
故选A.
本题解析:
本题难度:简单
5、填空题 (1)用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于?腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为?;
此反应每转移2mol电子消耗的O2在标准状况下的体积为?L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4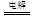 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是???。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是???。
参考答案:(1)吸氧? 2H2O+O2+4e-=4OH-? 11.2L
(2)如右图(图正确1分,标注1分)
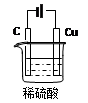
两极与电源的正负极接反了(或铜棒接电源的负极等)
本题解析:(1)红褐色锈斑的主要成分是Fe(OH)3,其主要是由于铁发生吸氧腐蚀时产生的。其发生的过程为:①正极反应:2H2O+O2+4e-=4OH-,负极反应:Fe-2e-=Fe2+;②4Fe(OH)2+2H2O+O2=4Fe(OH)3。由正极反应式可知,当转移2mol电子时,消耗的氧气的量为0.5mol,因此在标准状态下的体积为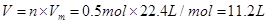 。
。
(2)由题可知,实现这一反应的装置应为电解池装置,且铜做为阳极。因此该装置图如下:
“某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀”铜棒没被腐蚀,说明此时铜棒应作为了阴极。
点评:本题综合考查了“原电池”与“电解池”等内容,属于基础题,也是高考的重要考点。本题的难点在于第二问对装置的判断。对于此种题型,应充分利用化学方程式,判断反应进行的难易以及氧化反应、还原反应,即可得出结论。
本题难度:一般