1������� ���������ĸߵ�ֱ��Ӱ�����������������������������ձ����п�����Ⱦָ������Ŀ�п�����������������������������ȡ�
(1)SO2��NO2��Ͽ�������������������÷�Ӧ�Ļ�ѧ����ʽΪ___________��
(2)�ҹ��о���Ա�����������õ�Ʒλ���̿���Ҫ�ɷ���MnO2������SO2���Ʊ������̣��÷�Ӧ�Ļ�ѧ����ʽΪ___________________��
(3)Ϊ�˼�ʱ��ؿ����ж�������ĺ�����ij��������ȡ100 L(��״����)������ͨ��װ�й�����ˮ��Һ������ƿ�У���ַ�Ӧ�������պ��ˮ��Һ�м���BaCl2��Һ�����ɰ�ɫ����0.1165 g����ÿ�����SO2���������Ϊ____��
�ο��𰸣�(1)SO2+NO2==SO3+NO
(2) SO2+MnO2==MnSO4
(3)0.0112��
���������
�����Ѷȣ�һ��
2��ѡ���� SO2ͨ���������ʵ���Һ�У�����ʹ����ɫ��ȥ����Ҫ����ΪSO2���л�ԭ���õ���
[? ]
A���Ȼ�ɫ��ˮ
B��Ʒ����Һ
C���Ϻ�ɫKMnO4������Һ
D�����Է�̪��Һ
�ο��𰸣�AC
���������
�����Ѷȣ���
3��ѡ���� ����������ȷ���ǣ�������
A��SO2��ʹ���������Һ��ɫ��˵��SO2��Ư����
B��ˮ������ͨCO2�ɵõ���״������˵��̼�����Աȹ���ǿ
C��Cl2��SO2���нϺõ�Ư�����ã�����Cl2��SO2��Ϻ������Ư��ֽ��
D��ij��Һ�м���BaCl2��Һ���а�ɫ�������ɣ���ϡ����������ܽ⣬֤����Һ�п϶�����SO42-
�ο��𰸣�A������������л�ԭ�ԣ����Ը��������ǿ�����ԣ������ܷ���������ԭ��Ӧ���������ӡ���������Ӷ�ʹ���Ը��������Һ��ɫ�������Ƕ��������Ư����ʹ���Ը��������Һ��ɫ����A����
B��ǿ���ܺ����������Һ��Ӧ�������ᣬˮ������ͨCO2�ɵõ���״�������ᣬ˵��̼�����Աȹ���ǿ����B��ȷ��
C��Cl2+SO2+2H2O=H2SO4+2HCl����������ᶼû��Ư���ԣ�����Cl2��SO2��Ϻ�����Ư��ֽ������C����
D���ܺ��Ȼ�����Һ��Ӧ���ɰ�ɫ�����ҳ���������ϡ�����������Ag+��SO42-��SO32-������ԭ��Һ�в�һ������SO42-����D����
��ѡB��
���������
�����Ѷȣ���
4������� ijͬѧ����ͼ��ʾװ��̽��SO2�����ʼ����й�ʵ�飮
��1��ʵ�������������ƹ����һ��Ũ�ȵ����ᷴӦ�Ʊ�SO2���壬д���÷�Ӧ�����ӷ���ʽ______
��2���ֱ�SO2����ͨ������C��Һ�У���ش��������⣺������SO2ͨ����ɫʯ����Һ��������______������ͨ�����SO2���壬������______��
��SO2ͨ����ɫKMnO4��Һ��������______���䷴Ӧ�����ӷ���ʽΪ______��
�۹���SO2������ͨ�����ʯ��ˮ�У�����______���ӷ���ʽ��______
����CΪ˫��ˮ����ͨ��SO2��������Һ��______?�������ʵĻ�ѧʽ��������ͬѧ�Ʊ���SO2�����л���CO2���壬�������ʵ�ԭ��������������ƹ����л���______��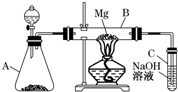
�ο��𰸣��𰸣���1���������ƺ����ᷴӦ���ɶ������������ƺ�ˮ�����ӷ���ʽΪ��SO32-+2H+�TSO2��+H2O��
�ʴ�Ϊ��SO32-+2H+�TSO2��+H2O��
��2���ٶ��������ˮ��Ӧ���������ᣬ�������ܵ���������ƶ��������ӣ�������Һ�����ԣ���ɫʯ����Һ������ɫ��������Һ���죻����������Ư���ԣ�������ʹʯ����ɫ�����Լ���ͨ�����SO2���壬�����Dz���ɫ�����ԣ�
�ʴ�Ϊ����죻����ɫ�����ԣ�
�ڶ��������л�ԭ�ԣ����������ǿ�����ԣ����Զ��������������ܷ���������ԭ��Ӧ��ʹ���������Һ��ɫ��dz����ɫ��ʧ�����ӷ�Ӧ����ʽΪ��5SO2+2MnO4+2H2O�T5SO42-+2Mn2++4H+��
�ʴ�Ϊ����ɫ�䵭����ɫ��ʧ��5SO2+2MnO4+2H2O�T5SO42-+2Mn2++4H+��
�۶���������������Ʒ�Ӧ���ɲ�����ˮ��������ƺ�ˮ��������ƺͶ�������ˮ�ܷ�Ӧ���ɿ����Ե���������ƣ����ӷ�Ӧ����ʽΪ��Ca2++2OH-+SO2=CaSO3 ��+H2O��CaSO3+SO2+H20=Ca2++2HSO3-��
�ʴ�Ϊ���ȱ���ǣ����ֱ���壻Ca2++2OH-+SO2=CaSO3 ��+H2O��CaSO3+SO2+H20=Ca2++2HSO3-��
�ܶ��������л�ԭ�ԣ�˫��ˮ��ǿ�����ԣ����Զ��������˫��ˮ�ܷ���������ԭ��Ӧ�������̼���κ�̼�������������ᷴӦ���ɶ�����̼������ͬѧ�Ʊ���SO2�����л���CO2���壬�������ʵ�ԭ��������������ƹ����л���̼���λ�̼�����Σ�
�ʴ�Ϊ��H2SO4��̼���λ�̼�����Σ�
���������
�����Ѷȣ�һ��
5��ѡ���� ���и��������У�ʹ��ɫ������ɫ�ķ�Ӧ������ͬ���ǣ�������
A�����������������
B����������ʹ�����
C�����������Ư��
D������̿�Ͷ�������
�ο��𰸣�B
���������
�����Ѷȣ�һ��