1、填空题 (10分)
(1)经测定,20g氢气在氧气中燃烧生成水蒸气,放热2418.0kJ,写出该反应的热化学方程式?;
已知:3Fe (s)+2O2(g)="=" Fe3O4(s)?△H=-1118.4kJ? mol―1,根据以上信息,则反应? 3Fe(s)+4H2O(g)==Fe3O4(s)+4H2(g)?的△H=?,该反应达平衡时,化学平衡常数表达式K=?。
(2)某学生实验小组用50mL0.50mol?L―1的盐酸与50mL0.50mol?L―1的NaOH溶液在下图所示的装置中进行中和反应反应热的测定

①图中装置缺少的一种仪器,该仪器名称为?。
②将反应混合液的?温度记为反应的终止温度。
③下列说法正确的是?
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅
C.烧杯间填满碎纸条的作用是固定小烧杯
D.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
参考答案:

本题解析:略
本题难度:简单
2、选择题 下列属于放热反应的是
A.铝和盐酸反应
B.焦碳和二氧化碳共热
C.石灰石的分解
D.氢气还原氧化铜
参考答案:A
本题解析:A属于放热反应,活泼的金属与酸反应放热;B吸热,焦碳和二氧化碳共热在高温条件反应;C吸热反应,大多数的分解反应为吸热反应;D,吸热反应;
本题难度:简单
3、填空题 (2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷)
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" ―1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g)?△H=" ―566" kJ/mol
则表示甲烷燃烧热的热化学方程式?。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是:?。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是?(填序号)
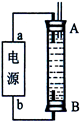
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)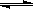 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
|
H2O
| CO
| CO2
|
1
| 650
| 2
| 4
| 1.6
| 5
|
2
| 900
| 1
| 2
| 0.4
| 3
|
3
| 900
| 1
| 2
| 0.4
| 1
|
?
①实验1中,以v (H2)表示的平均反应速率为?。
②实验3跟实验2相比,改变的条件可能是?(答一种情况即可)
参考答案:(1)CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1?
CO2(g)+2H2O(l) △H1=―890KJ.mol-1?
(2)CH4-8e-+ 10 OH- CO32-+ 7H2O;?
CO32-+ 7H2O;?
(3) B、D ;
(4)①? 0.16mol/(L・min)?②使用了催化剂;加大了压强(任答一种)
本题解析:
(1)甲烷完全燃烧生成二氧化碳气体和液态水,所以甲烷燃烧热的热化学方程式中甲烷的物质的量是1mol,将①②相加除以2可得,答案是CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1?
CO2(g)+2H2O(l) △H1=―890KJ.mol-1?
(2)负极发生氧化反应,所以甲烷在负极发生氧化反应,结合电解质溶液,负极的电极反应式为CH4- 8e-+ 10 OH- CO32-+ 7H2O;
CO32-+ 7H2O;
(3)A、电解过程中两极分别是H+和Fe放电生成氢气和亚铁离子,所以两极哪端都可以生成氢气,a不一定为正极,b不一定为负极,但a为正极,b为负极,效果较好,错误;B、在装置中铁一定作阳极,所以氯化钠溶液是电解质溶液,不影响阳极Fe放电生成亚铁离子,阴极H+放电生成氢气,正确;C、装置中铁一定作阳极,阴极可以是铁,也可以是其他惰性电极,错误;D、阴极H+放电生成氢气,正确,答案选BD。
(4)①实验1中,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= 0.8mol/L/5min=0.16mol/(L・min);
②实验3跟实验2相比,到达平衡时间缩短,说明反应速率加快,反应温度、各物质的物质的量均未变,所以可能是使用了催化剂或增大压强。
本题难度:一般
4、选择题 下列有关能量转换的说法不正确的是
[? ]
A.煤燃烧是化学能转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是化学能转变成热能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列反应既属于氧化还原反应,又是吸热反应的是(? )
A.铝和盐酸反应
B.灼热的木炭与CO2反应
C.氢气还原氧化铜
D.Ba(OH)2・8H2O晶体与NH4Cl晶体的反应
参考答案:BC
本题解析:A项为放热反应。D是复分解反应,不是氧化还原反应。故AD不能选。BC既是氧化还原反应,也是吸热反应,故选BC.
点评:本题综合了氧化还原反应和热化学反应知识点,侧重考查学生对相关概念的掌握,难度不大。
本题难度:一般