1��ѡ���� ijһ��ɫ����Ҫ�������Ƿ�I-�����в�����Ҫ����(����)
A������������ˮ�ܽ⣬�������ữ���ټ���AgNO3��Һ�۲�����������
B������NaOH��Һ�����ȣ�����������������
C������������ˮ�ܽ⣬�������ữ���ټ���BaCl2�۲�����������
D������������ˮ�ܽ⣬���������Һ������Һ������ɫ����
�ο��𰸣�A
���������A��ȷ��B����Ϊ����NH4+�ķ�����C����Ϊ����SO42���ķ�����D��������ⵥ�ʵķ�����
�����Ѷȣ�һ��
2��ѡ���� ���и�����ӦA��HCl����B��Cl2����C��NaClO����D��HClO����E��CO2�������в���һ��ֱ��ʵ�ֵ���(? )��
A��A��B
B��B��C
C��C��D
D��D��E
�ο��𰸣�D
���������MnO2��4HCl=MnCl2��Cl2��2H2O ��Cl2��2NaOH=NaCl��NaClO��H2O��NaClO��HCl=NaCl��HClO��������HClO������С��̼�ᣬ����ֱ������CO2
�����Ѷȣ���
3��ѡ���� ���¶��£���Cl2����ͨ��ˮ�������ͣ�Ȼ���ٵμ�0.1mol/L��NaOH��Һ,������������Һ��pH�仯������ͼ��ʾ������ѡ����ȷ����
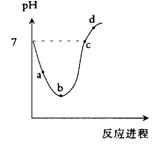
A��a����ʾ����Һ��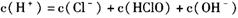
B��b����ʾ����Һ��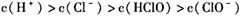
C��c����ʾ����Һ��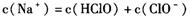
D��d����ʾ����Һ��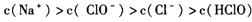
�ο��𰸣�B
���������������Һ������Ũ�ȴ�С�Ƚϡ�Aѡ�����a����Һ�Dz����͵���ˮ�����ݵ���غ㣬ʽ��C(HClO)����Ӧ��ΪC(ClO-)��Bѡ����ȷ��b���DZ�����ˮ�����з�Ӧ��������������ᣬ������ǿ����ʣ���������������ʣ�����������Ũ�����Bѡ����ȷ��Cѡ�����c��������Һ�����ݵ���غ�ɵù�ϵc(Na+)=c(Cl-)+c(ClO-)������c���������뷴Ӧ��������c(ClO-)��c(Cl-)���ȣ�����Cѡ�����D�����������Ȼ�����������ƻ��Һ��c(ClO-)�����ܱ�c(Cl-)��ѡB��
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
A�������к����������Ȼ��⣬������NaOH��Һ��ȥ
B��Ư�۵���Ч�ɷ���CaCl2��Ca(ClO)2
C����ʪ����������Ũ������и���
D��ʵ������ȡ����ʱ���������ſ������ռ�
�ο��𰸣�CD
���������A�����������Ƽ�����������Ӧ�������Ȼ��ⷴӦ��B����Ư�۵���Ч�ɷ���Ca(ClO)2
�����Ѷȣ���
5��ѡ���� ��������ˮ�Dz������������ģ�Ϊ��������ˮ��Cl�C�Ĵ��ڣ����ѡ�����������е� (? )
A��ʯ����Һ
B�����Ȼ�̼
C������������Һ
D����������Һ
�ο��𰸣�D
���������������������Һ�����ְ�ɫ���������ǣ�˵����Cl�C�Ĵ��ڣ���D��ȷ��
�����Ѷȣ���