1、选择题 已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-均有相同的电子层结构,则下列叙述正确的是( )
A.原子序数:a>b>c>d? B.离子还原性:A(n+1)+>Bn+,离子氧化性:C(n+1)->Dn- ?
C.离子半径:A(n+1)+>Bn+>C(n+1)->Dn-?D.单质还原性:B>A,单质氧化性:D>C
参考答案:D
本题解析:略
本题难度:一般
2、选择题 下列各原子或离子的电子排布式错误的是(?)。
A.C 1s22s22p2
B.O2- 1s22s22p6
C.Cr 1s22s22p63s23p63d44s2
D.Al3+ 1s22s22p6
参考答案:C
本题解析:本题C选项铬原子的电子排布式违反了洪特规则的特例,正确排布为:1s22s22p63s23p63d54s1。
本题难度:一般
3、选择题 下列说法中正确的是
A.只含有非金属元素的化合物可能是离子化合物
B.第ⅠA族元素都比第ⅡA族元素金属性强
C.只含有共价键的物质一定是共价化合物
D.同主族元素原子半径越小越容易失去电子
参考答案:A
本题解析:A、只含有非金属元素的化合物可能是离子化合物,例如铵盐等,A正确;B、同周前第ⅠA族元素都比第ⅡA族元素金属性强,B不正确;C、只含有共价键的物质不一定是共价化合物,也可能是单质,C不正确;D、同主族元素原子半径越大越容易失去电子,D不正确,答案选A。
本题难度:一般
4、选择题 下列各种说法中,正确的是 ?( )
A.3号到9号元素化合价的变化与11到17号元素化合价的变化完全相同
B.同周期原子半径逐渐减小,所以离子半径也逐渐减小
C.随着原子序数的递增,碱金属元素单质的还原性逐渐增强,阳离子的氧化性逐渐减弱
D.甲乙电子层数相同,甲的最高价氢氧化物的碱性比乙的最高价氢氧化物的碱性强,说明甲的核电荷数比乙大
参考答案:C
本题解析:A.与11到17号元素化合价的变化规律基本重复3号到9号元素化合价的变化。但是8号元素O、9号元素F无正价,而16号元素S、17号元素Cl则有+6、+7价。错误。B.同周期原子半径逐渐减小,但是同一周期的金属元素形成的离子是上一周期是惰性气体的原子结构;同一周期的非金属元素形成的阴离子为同一周期是该周期的惰性气体的原子结构。比该周期的计算元素的离子多一个电子层。半径比金属离子的大。对于对称层结构相同的微粒来说,核电荷数越大,离子半径越小;对于电子层结构不同的微粒来说,电子层数越多,离子半径越大。错误。C.同一主族的元素,从上到下,随着原子序数的递增,原子半径逐渐增大,碱金属元素单质的还原性逐渐增强,阳离子的氧化性逐渐减弱。正确。D.甲乙电子层数相同,甲的最高价氢氧化物的碱性比乙的最高价氢氧化物的碱性强,说明甲的核电荷数比乙小。错误。
本题难度:一般
5、选择题 下列图示正确的是
A.氟化氢的电子式: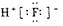
B.次氯酸的结构式:H―Cl―O
C.铝离子的结构示意图: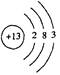
D.氯化铯的晶体结构(晶胞)模型: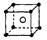
参考答案:D
本题解析:氟化氢为共价化合物;次氯酸的成键方式H―O―Cl;铝离子只有两层电子。
本题难度:一般