1、选择题 下列反应中,是吸热反应的是(? )
A.铁片与稀硫酸反应
B.甲烷在空气中燃烧
C.单质钠与水反应
D.Ba(OH)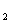 ・8H
・8H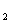 O晶体与氯化铵晶体反应
O晶体与氯化铵晶体反应
参考答案:D
本题解析:考查常见的放热反应和吸热反应。一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。所以答案是D。
本题难度:简单
2、填空题 (16分)
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g)
2SO3(g)
(1)此反应是工业上生产?的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是?(填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
①根据有关数据,请分析在工业生产中选择常压反应器的原因:
?。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g)?△H=?。
2SO3(g)?△H=?。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下:

①求该温度时,氨水的电离平衡常数K=?。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
①? a ??b?(填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3・H2O)=?。
(用含有a、b的式子表示)
参考答案:(16分,每空2分)
I.(1)硫酸 (或者H2SO4)?
(2)a d
(3)①在常压下,此反应的转化率已经达到96%,没有必要再增大压强了。
②-396.00 kJ/mo1
Ⅱ.(1)① 4.00×10-4
②
(2)① <? ② 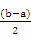
本题解析:I.(1)二氧化硫的催化氧化是工业生产硫酸的重要步骤;
(2)a、每生成1mol SO3的同时生成0.5mol O2,代表正逆两个反应方向且符合化学方程式中的系数比,符合正逆反应速率相等,达到平衡状态,正确;b、恒容条件下,气体的质量不变,所以气体的密度一直不变,不能判断是否达平衡状态,错误;c、体系中各物质的物质的量之比等于化学计量数之比时不一定达平衡状态,错误;d、该反应的特点是反应前后的气体的物质的量发生改变,所以恒容时气体的压强在变,达平衡时,气体压强不再变化,正确,答案选ac。
(3)①常压下,平衡时二氧化硫的转化率是96%,已经很高,所以没有必要再增大压强了;
②二氧化硫转化96%放出190.08KJ的热量,所以1mol二氧化硫气体完全反应则放出190.08kJ÷96%=198.00kJ的热量,所以该反应的热化学方程式中二氧化硫的系数是2,代表2mol的二氧化硫完全反应,放出的热量是198.00kJ×2=396.00kJ,所以△H=-396.00 kJ/mo1;
II.(1)①根据题意可知氨水的浓度是1mol/L, c(NH4+)= c(OH-)=0.02mol/L,所以氨水的电离常数K= c(NH4+)・ c(OH-)/c(NH3・H2O)= 0.022mol/L/1mol/L= 4.00×10-4
②氨水稀释会促进一水合氨的电离,体积变为原来的2倍,则氢氧根离子浓度减小为原来的一半,根据勒夏特列原理,最终氢氧根离子、铵根离子的浓度仍会减小,所以图像的起点在0.01处,最大值在原图像的下方,如图 ;
;
(2)①若a=b,则二者恰好完全反应,溶液呈酸性,现在溶液呈中性,说明氨水过量,所以a<b;
②设二者的体积均是1L,因为b>a,则剩余氨水的物质的量是b-a,体积扩大到原来的2倍,所以剩余氨水浓度:c(NH3・H2O)=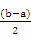 。
。
本题难度:一般
3、填空题 合成氯是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g)  2NH3(g) ΔH=-93.0kJ/mol
2NH3(g) ΔH=-93.0kJ/mol
(1)某温度下,在2 L密闭容器中发生上述反应,测得数据如下
?时间/h
物质的量/mol
| 0
| 1
| 2
| 3
| 4
|
N2
| 2.0
| 1.83
| 1.7
| 1.6
| 1.6
|
H2
| 6.0
| 5.49
| 5.1
| 4.8
| 4.8
|
NH3
| 0
| 0.34
| 0.6
| 0.8
| 0.8
|
?
①0~2 h内,v(N2)=?。
②平衡时,H2的转化率为____;该温度下,反应2NH3(g)  ?N2(g)+3H2(g)的平衡常数K=?。
?N2(g)+3H2(g)的平衡常数K=?。
③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同的为?(填选项字母)。
A.a=l、b=3.c=0?B.a=4、b=12、c=0
C.a=0、b=0.c=4?D.a=l、b=3、c=2
(2)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热ΔH=-286kJ/mol,则陪制NH3反应的热化学方程式为?。
(3)采用高质子导电性的SCY陶瓷(能传递H"),通过电解法也可合成氨,原理为:
N2(g)+3H2(g)  2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?___极,该电极反应式为?。
2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?___极,该电极反应式为?。
参考答案:(1)①0.075 mol・L-1・h-1?②20%? 69.12?③C D?
(2)2 N2(g) + 6 H2O (l) =" 4" NH3(g) + 3 O2 (g) ΔH =" +1530" kJ・mol-1
(3)阴? N2 + 6 H+ + 6e- = 2NH3
本题解析:
?
?试题分析:(1)①v(N2)= ?c(N2) ÷?t =(2.0-1.7)mol÷2L÷2h=0.075mol/(L・h) ②平衡时,H2的转化率为(6.0-4.8) ÷6.0×100%=20%.化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数的乘积的比。所以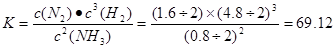 。③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同,则应该一边倒转化,得到的N2物质的量为2mol,H2的物质的量为6mol,NH3的物质的量为0mol。可知C、D符合要求。选项为C、D。①N2(g)+3H2(g)
。③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同,则应该一边倒转化,得到的N2物质的量为2mol,H2的物质的量为6mol,NH3的物质的量为0mol。可知C、D符合要求。选项为C、D。①N2(g)+3H2(g)  2NH3(g)?H=-93.0KJ/mol; ②2H2(g)+O2(g)=2H2O(l) ?H=-572KJ/mol.①×2-②×3.整理可得:2 N2(g) + 6 H2O (l) =" 4" NH3(g) + 3 O2 (g) ΔH =" +1530" kJ/mol。(3)因为N2在反应中得到电子,化合价降低,所以应该把N2不断地通入阴极。电极反应式为N2 + 6 H+ + 6e- = 2NH3。考点:
2NH3(g)?H=-93.0KJ/mol; ②2H2(g)+O2(g)=2H2O(l) ?H=-572KJ/mol.①×2-②×3.整理可得:2 N2(g) + 6 H2O (l) =" 4" NH3(g) + 3 O2 (g) ΔH =" +1530" kJ/mol。(3)因为N2在反应中得到电子,化合价降低,所以应该把N2不断地通入阴极。电极反应式为N2 + 6 H+ + 6e- = 2NH3。考点:
本题难度:一般
4、选择题 下列化学反应属于吸热反应的是(?)
A.碘的升华
B.生石灰溶于水
C.镁与稀盐酸反应
D.氢氧化钡与氯化铵晶体混合
参考答案:D
本题解析:考查常见的放热反应和吸热反应。一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。所以答案选D。
本题难度:简单
5、选择题 下列热化学方程式书写正确的是(?)
A.C(s)+O2(g)=CO2(g)ΔH=+393.5 kJ/mol
B.2SO+O2=2SO3ΔH=-196.6 kJ/mol
C.H2(g)+1/2O2(g)=H2O(l)ΔH=-285.8 kJ/mol
D.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ
参考答案:C
本题解析:C的燃烧反应为放热反应,A错;书写热化学方程式需要带状态,B错;ΔH的单位为kJ・mol-1,D错。
本题难度:一般