1、选择题 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+
O2(g)═CO2(g)+2H2(g);△H=-192.9kJ?mol-1
下列说法正确的是( )
A.CH3OH的燃烧热为192.9kJ?mol-1
B.反应①中的能量变化如图所示
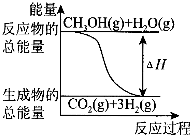
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ?mol-1
2、选择题 化学反应的发生必然伴随有能量的转化,其根本原因是( )
A.化学反应中一定有新物质生成
B.化学反应中旧化学键的断裂需要吸收能量,新化学键的生成需要放出能量
C.化学反应通常需要加热等条件才能发生
D.生成物的总能量与反应物的总能量不同
3、填空题 (3分)不同的物质不仅组成不同、结构不同 ,所包含的?也不同。放热反应的宏观表现是?,其微观表现是?。
,所包含的?也不同。放热反应的宏观表现是?,其微观表现是?。
4、选择题 下列说法正确是( )
A.由H原子形成1molH-H键要吸收热量
B.在稀溶液中,酸与碱发生中和反应生成H2O时所释放的热量称为中和热
C.N2性质非常稳定,是因为N2分子中含有氮氮叁键,要破坏氮氮叁键需吸收更多的能量
D.凡经加热而发生的化学反应都是吸热反应
5、选择题 下列说法中,正确的是(? )
A.△H>0表示放热反应,△H<0表示吸热反应
B.M与N是同素异形体,由M=N;△H=+119KJ/mol可知,M比N稳定
C.l mol H2SO4与1mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热