1、选择题 已知:在25℃时,?H2O H++OH- ?KW=10-14 ?
H++OH- ?KW=10-14 ?
CH3COOH H++CH3COO- ?Ka=1.8×10-5?
H++CH3COO- ?Ka=1.8×10-5?
KSP[Mg(OH)2]=1.8×10-11?
?KSP[Zn(OH)2]=1.2×10-17、
KSP[Cd(OH)2]=2.5×10-14?
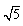 ?=2.2 下列说法正确的是
?=2.2 下列说法正确的是
[? ]
A.醋酸钠水解的平衡常数Kh随温度升高而减小
B.0.5mol・L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a;1mol・L-1醋酸钠溶液pH为n,水解的程度为b,则m<n?、?a>b ?
C.醋酸钠的水解的平衡常数Kh=?KW?Ka ?
D.在某溶液中含Mg2+、Cd2+、Zn2+三种离子的浓度均为0.01mol・L-1?,向其中加入固体醋酸钠,使其浓度为0.9mol・L-1,以上三种金属离子中只有Zn2+?能生成沉淀
参考答案:B
本题解析:
本题难度:一般
2、选择题 已知常温下:Ksp〔Mg(OH)2〕=1.8×10-11,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12 ,
Ksp(CH3COOAg)=2.3×10-3。下列叙述正确的是
[? ]
A.等体积混合浓度均为0.2 mol・L-1的AgNO3溶液和CH3COONa溶液一定产生CH3COOAg沉淀
B.将0.001 mol・L-1的AgNO3溶液滴入0.001 mol・L-1的KCl和0.001 mol・L-1的K2CrO4溶液中,先产生Ag2CrO4沉淀
C.在Mg2+为0.121 mol・L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上
D.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大
参考答案:AC
本题解析:
本题难度:一般
3、填空题 (13分)高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:

根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式 。
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10―38,除杂后溶液中c(Fe3+)约为 。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是 & #160; 。
(5)“分离”操作的名称是 (填字母代号)。
A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2・12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是 ,离子浓度最小的离子是 。
参考答案:(13分) (1) 2Fe2++H2O2+4NH3・H2O=2Fe(OH)3↓+4NH4+
(2)4×10―20mol/L(3分)。(3)抑制(防止)Al3+水解。(2分)
(4)防止晶体失去结晶水,避免可溶性杂质结晶析出(2分,答对1点给1分)。
(5)C(1分)。(6)SO42―,OH―。(共2分,各1分)
本题解析:(1)H2O2可以把Fe2+氧化为Fe3+,然后加入氨水,就会形成Fe(OH)3沉淀而过滤除去,反应的离子方程式是2Fe2++H2O2+4NH3・H2O=2Fe(OH)3↓+4NH4+;(2)pH=8.0,则c(OH―)=10-6mol/L,在通常条件下Ksp〔Fe(OH)3〕=c(Fe3+)・c3(OH―)=4.0×10―38,所以c(Fe3+)= Ksp〔Fe(OH)3〕÷c3(OH―)= 4.0×10―38÷10-18=4×10―20mol/L;(3)硫酸铝是强酸弱碱盐,水解产生氢氧化铝胶体和硫酸,加入硫酸就可以抑制盐电离产生的Al3+的水解;(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干是因为蒸干容易使晶体失去结晶水,这样还避免可溶性杂质结晶析出;(5)把晶体从混合物中“分离”操作的名称是过滤;(6)铵明矾晶体的化学式为NH4Al(SO4)2・12H2O,在0.1mol/L在铵明矾的水溶液中,根据物料守恒可知离子浓度最大的离子是SO42―,由于该盐是强酸弱碱盐,NH4+、Al3+水解消耗水电离产生的OH-,使溶液显酸性,所以离子浓度最小的离子是OH―。
考点:考查物质制取的知识,包括反应条件的选择、离子方程式的书写、溶度积常数的应用、盐的水解、离子浓度的大小比较的知识。
本题难度:困难
4、填空题 (14分)某工业原料主要成分是NH4Cl、FeCl3和AlCl3。利用此原料可以得到多种工业产品。分析下面流程,回答问题。
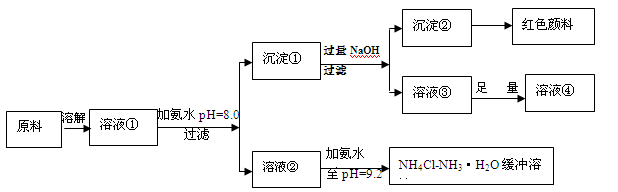
已知:Ksp[Fe(OH)3]=4.0×10-38
(1)用稀硫酸中和等体积等pH值的氨水和烧碱溶液,前者需要消耗的酸液体积 (填“大”“小”或“相同”)
(2)计算溶液②中Fe3+的物质的量浓度为 mol/L
(3)缓冲溶液中存在的平衡体系有: 、 、
此时溶液中c(NH4+) c(Cl-)(填>、=、<)。
(4)在缓冲溶液中加入少量盐酸或者NaOH溶液,溶液的pH值几乎依然为9.2。简述原理:
请举出另一种缓冲溶液的例子(写化学式) 。
(5)常温下向较浓的溶液④中不断通入HCl气体,可析出大量AlCl3・6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
参考答案:(1)大 (2分)
(2)4.0×10-20 (2分)
(3)NH4++H2O NH3・H2O+H+(Ⅰ) NH3・H2O
NH3・H2O+H+(Ⅰ) NH3・H2O NH4++OH-(Ⅱ) H2O
NH4++OH-(Ⅱ) H2O H++OH-(Ⅲ) >
H++OH-(Ⅲ) >
(4分,每空1分)
(4)当加入少量酸时,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。(2分)
CH3COONa-CH3COOH(或其它合理答案) (1分)
(5)AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s) Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。(3分)
Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。(3分)
(从抑制铝离子水解角度答题不得分)
本题解析:(1)pH相同的氨水和烧碱,氨水的物质的量浓度大,所以需要的酸的体积大。(2) 溶液的pH=8,氢离子浓度=10-8mol/L,氢氧根离子浓度=10-6mol/L,根据Ksp[Fe(OH)3]=4.0×10-38计算铁离子浓度=4.0×10-20。
(3)缓冲溶液中有铵根离子,所以存在铵根离子的水解平衡,NH4++H2O NH3・H2O+H+,溶液中有一水合氨,NH3・H2O
NH3・H2O+H+,溶液中有一水合氨,NH3・H2O NH4++OH-,存在一水合氨的电离平衡,溶液中肯定存在水的电离平衡, H2O
NH4++OH-,存在一水合氨的电离平衡,溶液中肯定存在水的电离平衡, H2O H++OH-。由于溶液中的pH=9.2,所以溶液显碱性,说明氢离子浓度小于氢氧根离子浓度,根据电荷守恒,所以铵根离子浓度大于氯离子浓度。(4)缓冲溶液中加入少量盐酸,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。类似的缓冲溶液由CH3COONa-CH3COOH。 (5) 沉淀①为氢氧化铝和氢氧化铁,加入过量氢氧化钠后溶液③为偏铝酸钠,沉淀②为氢氧化铁沉淀,溶液③中加入足量的盐酸,得到的溶液④为氯化铝溶液,在AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s)
H++OH-。由于溶液中的pH=9.2,所以溶液显碱性,说明氢离子浓度小于氢氧根离子浓度,根据电荷守恒,所以铵根离子浓度大于氯离子浓度。(4)缓冲溶液中加入少量盐酸,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。类似的缓冲溶液由CH3COONa-CH3COOH。 (5) 沉淀①为氢氧化铝和氢氧化铁,加入过量氢氧化钠后溶液③为偏铝酸钠,沉淀②为氢氧化铁沉淀,溶液③中加入足量的盐酸,得到的溶液④为氯化铝溶液,在AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s) Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。
Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。
考点:盐类的水解。
本题难度:困难
5、选择题 下列说法正确的是(? )
A.水的离子积常数Kw随温度改变而改变,随外加酸碱浓度改变而改变
B.一元弱酸的电离常数Ka越小,表示此温度下该一元弱酸电离程度越大
C.对已达到化学平衡的反应,仅改变浓度,若平衡移动则平衡常数(K)一定改变
D.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
参考答案:D
本题解析:A项,水的离子积常数Kw只与温度有关,不随外加酸碱浓度的改变而改变,故A错误;B项,电离常数Ka是表示弱电解质电离程度大小的物理量,Ka值越大,表示该一元弱酸电离程度越大,B错误;C项,平衡常数(K)只与温度有关,与浓度无关,故C错误。
本题难度:一般