1、填空题 (8分)W、X、Y、Z四种化合物的焰色反应均为黄色,它们之间存在如下关系:
①W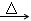 X+CO2↑+H2O
X+CO2↑+H2O
②Z+CO2 X+O2
X+O2
③Z+H2O Y+O2↑
Y+O2↑
④X+Ca(OH)2 Y+CaCO3↓
Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:
W?、X?、Y?、Z?。
(2)以上4个化学反应,属于氧化还原反应的是?(填反应序号),反应中氧化剂是
?(写化学式),还原剂是?(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应方程式:
①?。②?。
参考答案:(1)NaHCO3? Na2CO3? NaOH? Na2O2?(2)②③? Na2O2? Na2O2
(3)①Ca2++CO32-=CaCO3↓? ②Ca(OH)2+K2CO3=2KOH+CaCO3↓(合理即可)
本题解析:四种化合物的焰色反应均为黄色,四种化合物均为钠的化合物。①反应可认定为
NaHCO3的分解反应:2NaHCO3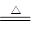 Na2CO3+CO2↑+H2O,该反应是非氧化还原反应。由X(Na2CO3)逆推可知Z为Na2O2,Y为NaOH:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,以上两个反应都是氧化还原反应,且Na2O2既是氧化剂又是还原剂。这样,④反应为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,其离子反应为Ca2++CO32-=CaCO3↓,多数可溶性碳酸盐和Ca(OH)2的反应都可用此离子方程式表示,该反应不是氧化还原反应。
Na2CO3+CO2↑+H2O,该反应是非氧化还原反应。由X(Na2CO3)逆推可知Z为Na2O2,Y为NaOH:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,以上两个反应都是氧化还原反应,且Na2O2既是氧化剂又是还原剂。这样,④反应为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,其离子反应为Ca2++CO32-=CaCO3↓,多数可溶性碳酸盐和Ca(OH)2的反应都可用此离子方程式表示,该反应不是氧化还原反应。
本题难度:一般
2、填空题 (12分)现有失去标签的氯化钙,硝酸银,盐酸,碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编号上A.B.C.D后,产生的现象如下表所示:
| 实验内容
| 实验现象
|
(1)
| A+B
| 没有现象发生
|
(2)
| B+D
| 有气体放出
|
(3 ) )
| B+C
| 有沉淀生成
|
(4)
| A+D
| 有沉淀生成
|
根据实验现象按要求回答:
(1)写出A.B.C.D溶液中溶质的化学式:
A______? B_______? C_____? D______
(2)写出上述实验中有关反应的离子方程式
实验(2) B+D ___________________? ?
?
实验(3) B+C __________________
参考答案:(12分)(1)A__CaCl2_ ?B__ HCl__? C__AgNO3 __? D_Na2CO3___
(2)实验(2) B+D ____ CO32-+2H+=H2O+CO2↑_________?
实验(3) B+C ________ Ag++Cl-="?" AgCl ↓________
本题解析:略
本题难度:一般
3、推断题 已知在如图转化关系(某些转化关系中的产物已略去)中都是中学化学常见的物质,物质A、D、G是单质,F是混合物,黑色物质C是某金属矿物的主要成分,有磁性,E是一种非氧化性酸,H是极易溶于水的碱性气体。

请回答下列问题:
(1)写出下列物质的化学式:A_______、C_______、I_______
(2)写出反应①的化学方程式:_________________
(3)在一定温度、压强和有催化剂存在的条件下将1molG和 2.5molD放入500mL密闭容器中。经过20min达到平衡,平衡后H的浓度为2mol/L,则用G表示20min内的平均反应速率为____,该温度下此反应的平衡常数K=___, D的转化率为____。如果保持温度不变,再向容器中同时充入1.5molG和1molH,D的转化率将___(填“升高”“不变”或“降低”),再次平衡后H的体积分数为____。
参考答案:(1)Fe;Fe3O4;Fe(OH)3
(2)3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
(3)0.05mol・L-1・min-1;0.5;60%;不变;40%
本题解析:
本题难度:一般
4、简答题 有含钠元素的两种物质A和B,它们与化合物F的反应分别是A+F→C+D↑;B+F→C+E↑,又知常温下D和E两种气体可以体积之比1:2化合成液态化合物F.经分析知A中含有D中的非金属元素,B为金属钠与E中的元素化合成的摩尔质量为24g/mol的固体.试回答下列问题:
(1)写出化学式.A______;B______;C______;D______;E______;F______.
(2)写出化学反应方程式:A+F______;B+F______.
参考答案:由题意可知液态化合物F为H2O,则D为O2,E为H2,B为金属钠与E中的元素化合生成的固体,结合B的摩尔质量可知B为NaH,进一步可推知A为Na2O2,C为NaOH,
(1)由以上分析可知A:Na2O2? B:NaH? C:NaOH? D:O2? E:H2? F:H2O,
故答案为:Na2O2;NaH;NaOH;O2;H2;H2O;
(2)Na2O2和H2O反应生成NaOH和O2,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,NaH和H2O反应生成NaOH和H2,反应的化学方程式为NaH+H2O=NaOH+H2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;NaH+H2O=NaOH+H2↑.
本题解析:
本题难度:一般
5、填空题 反应①②是重要的化工反应,D、E、F、G为单质,D、E、G、H为气体,且只有E为有色气体,F是常见的金属单质,G是空气中主要成分之一,K是白色胶状沉淀,C的焰色反应为黄色,其物质间的转化关系如下,虚框内是需设计的内容,反应物只能用A~J中的物质:
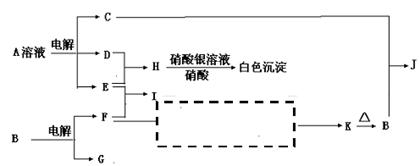
(1)A的电子式?, H的结构式是?;
(2)A溶液的电解方程式是?;
C+B→J的离子方程式是?;
(3)请设计F→K的最佳途径
(4)按设计得到1mol K,电解B时转移的电子数目是?,至少需要另加试剂的物质的量是?:?mol,?:?mol,?:?mol(可不填满)。
参考答案:(1)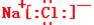 ?H―Cl ?
?H―Cl ?
(2) 2NaCl+2H2O=2NaOH+Cl2↑+H2↑、Al2O3+2OH―=2AlO2―+H2O
(3)

(4)1.8×1024,HCl 0.25mol,NaOH 0.75mol
本题解析:略
本题难度:简单