1、填空题 (6分)某温度时,在容积为2L的密闭容器中,三种气体物质的量随时间的变化曲线如图所示。请根据图中数据作答。
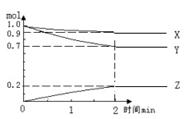
①列式计算在2分钟内X的化学反应速率?
②写出该反应的化学方程式?
③达到平衡时,Y的转化率为?
2、选择题 对可逆反应2A(s)+3B(g)  ?C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
?C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v (正)、v(逆)不变?
④增大B的浓度,v(正)>v(逆)?⑤加入催化剂,B的转化率提高
A.①②
B.④
C.③
D.④⑤
3、填空题 (6分)(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) CO2(g)十H2 (g),△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=?mol/(L・min),此时该反应的平衡常数为?。
CO2(g)十H2 (g),△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率υ(CO)=?mol/(L・min),此时该反应的平衡常数为?。
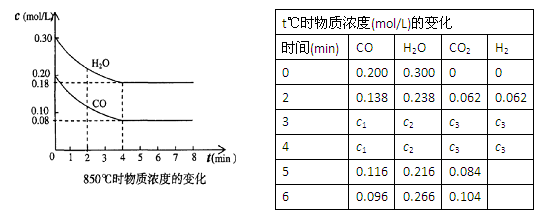
(2)T ℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于? ?状态;c1?0.08 (填 “>”、“<”或“=”)。
?状态;c1?0.08 (填 “>”、“<”或“=”)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是?(填序号,下同),表中5min~6min之间数值发生变化,可能的原因是?。
a.增加了水蒸气的量? b.降低温度
c.使用催化剂? d.增加氢气的浓度
4、填空题 捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)  ?(NH4)2CO3(aq)ΔH1
?(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)  NH4HCO3(aq)ΔH2
NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)  2NH4HCO3(aq)ΔH3
2NH4HCO3(aq)ΔH3
请回答下列问题:
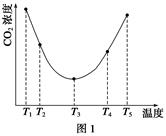
(2)为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图1)。则:
①ΔH3________0(填“>”、“=”或“<”)。
②在T1~T2及T4~T5两个温度区间,容器内CO2气体浓度呈现如图1所示的变化趋势,其原因是____________________________________________________________________________。
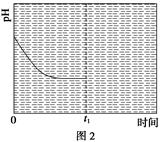
③反应Ⅲ在温度为T1时,溶液pH随时间变化的趋势曲线如图2所示。当时间到达t1时,将该反应体系温度迅速上升到T2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化总趋势曲线。
(3)利用反应Ⅲ捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有________________________(写出2个)。
(4)下列物质中也可能作为CO2捕获剂的是__________。
A.NH4Cl
B.Na2CO3
C.HOCH2CH2OH
D.HOCH2CH2NH2
5、计算题 合成氨工厂常通过测定反应前后混合气体的密度来确定氮的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L。若N2、H2起始时总物质的量为1mol,求该合成氨厂N2的转化率。