| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《认识晶体》练习题(一)
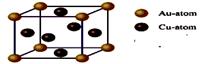 ①钴原子在基态时,核外电子排布式为:____________。 ②乙醇沸点比氯乙烷高,主要原因是____________。 ③上图是金与铜形成的金属互化物合金,它的化学式可表示为:________。 ④含碳源中属于非极性分子的是___(a.甲烷? b.乙炔? c.苯? d.乙醇) ⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:________。 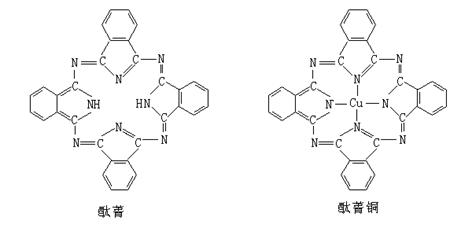 2、选择题 下列关于晶体的叙述中,不正确的是……( ) 3、填空题 (10分)已知有关物质的熔、沸点数据如下表:
(2)请设计可靠的实验证明MgCl2、AlCl3所属化合物的类型,其实验方法是_____▲____ 。 (3)AlCl3具有以下__▲__特殊性质(请填序号)。①液化②挥发③升华 4、选择题 碳化硅(SiC)俗称金刚砂,常用作砂轮及高温炉的材料,它不导电,由此可以推知碳化硅属于(?) 5、选择题 下列物质在固态时是由原子直接构成的是( ) |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《大气污染与.. | |