1、填空题 (6分)有a、b两个等体积且极易导热的密闭容器,a保持容积不变,b中的活塞可上下移动,以保持内外压强相等。在相同条件下将3mol A,1mol B分别同时混合于a、b两容器中,发生反应:3A(g)+B(g)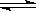 2C(g)+D(g)
2C(g)+D(g)
(1)达到平衡时,a中A的浓度为M mol/L。A的转化率为N,b中A的浓度为m mol/L,A的转化率为n,则M____m;N_____n(填>、<、=、无法比较)
(2)保持温度不变,按下列配比分别充入a、b两容器,达平衡后,a中A的浓度为M mol・L-1的是?
A? 6mol A+2mol B? B? 3mol A+2mol C? C? 2mol C+1mol B+1mol D
D? 2mol C+1mol D? E? 1.5mol C+0.5mol B+1mol C+0.5mol D
参考答案:(1)<?<?(2)D、E
本题解析:(1)反应是一个体积减小的可逆反应。在反应过程中b中的压强始终大于a中的压强,所以b中的转化率大于a中的。由于b的体积小,所以A的浓度大于a中的。
(2)a是保持体积不变的,所以要使平衡等效,则换算后的物质的物质的量和最初的相同。选项C相当于3mol A+2mol B,选项D相当于是3mol A+1mol B,选项E相当于是3mol A+1mol B,所以答案是DE。
本题难度:一般
2、选择题 工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2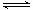 2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
A.使用催化剂是为了加快反应速率,提高生产效率
B.在上述条件下,SO2不可能100%地转化为SO3
C.达到平 衡时,改变反应条件可能在一定程度上改变该反应的化学平衡状态
D.达到平衡时,SO2的浓度与SO3的浓度一定相等
参考答案:D
本题解析:使用催化剂是为了加快反应速率,提高生产效率,A正确;该反应是可逆反应,所以在上述条件下,SO2不可能100%地转化为SO3,B正确;平衡状态是一定条件下的,如果改变外界条件,平衡状态可以发生变化,C正确;在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此选项D不正确,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。侧重考查学生对可逆反应平衡状态特点以及外界条件对平衡状态影响的熟悉了解程度,有利于调动学生的学习兴趣,提高学生的学习效率和应试能力。
本题难度:一般
3、选择题 一密闭烧瓶中装有NO2气体,在一定条件下达到化学平衡2NO2 ?N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是?
?N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是?
A.颜色不变
B.颜色变浅
C.颜色加深
D.无法判断
参考答案:C
本题解析:略
本题难度:一般
4、选择题 下列可逆反应中,正反应是吸热反应的是
A.PCl3(l)+Cl2(g) PCl5(s) 降温,PCl3转化率增大
PCl5(s) 降温,PCl3转化率增大
B.NO2(g)+SO2(g) NO(g)+SO3(g) 降温,SO3的体积分数增加
NO(g)+SO3(g) 降温,SO3的体积分数增加
C.2NO2 (g) 2NO(g)+O2(g) 降温,颜色加深
2NO(g)+O2(g) 降温,颜色加深
D.CS2(l)+2H2O(g) CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
参考答案:CD
本题解析:A、降温,PCl3转化率增大,平衡正向移动,正反应放热;
B、降温,SO3的体积分数增加,平衡正向移动,正反应放热;
C、降温,颜色加深,平衡逆向移动,逆向放热,正向吸热;
D、升温,CO2的平衡浓度增大,平衡正向移动,正向吸热。
本题难度:一般
5、选择题 某温度下在固定体积的密闭容器中发生如下反应:2M(g)+N(g) 2E(g),若开始时只充入2molE(g),达到平衡时,混合气体的压强比起时增大了20%;若开始时只充入2molM和1molN的混合气体,达到平衡时M的转化率为
2E(g),若开始时只充入2molE(g),达到平衡时,混合气体的压强比起时增大了20%;若开始时只充入2molM和1molN的混合气体,达到平衡时M的转化率为
[? ]
A.20%?
B.40%?
C.60%?
D.80%
参考答案:C
本题解析:
本题难度:一般