1��ѡ���� ��Fe2����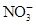 ��Fe3����
��Fe3����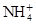 ��H2O��H���������ӣ��ֱ�����ͬһ������ԭ��Ӧ�еķ�Ӧ�����������������������(? )
��H2O��H���������ӣ��ֱ�����ͬһ������ԭ��Ӧ�еķ�Ӧ�����������������������(? )
A���������뻹ԭ�������ʵ���֮��Ϊ8��1
B����ԭ����Ϊ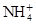
C������1 mol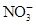 �μӻ�ԭ��Ӧ��ת��8 mol e��
�μӻ�ԭ��Ӧ��ת��8 mol e��
D�����Ѹ÷�Ӧ���Ϊԭ��أ�����ӦΪFe2����e��=Fe3��
�ο��𰸣�A
������������������ӵ������жϷ�Ӧ����������Ӧ��ӦΪFe2+��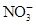 ��H+��������ӦΪFe3+��
��H+��������ӦΪFe3+��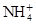 ��H2O�����õ�ʧ�����غ㣬��ƽ����ʽ��8Fe2����
��H2O�����õ�ʧ�����غ㣬��ƽ����ʽ��8Fe2����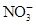 ��10H��=8Fe3����
��10H��=8Fe3����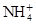 ��3H2O��������
��3H2O��������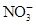 �뻹ԭ��Fe2�������ʵ���֮��Ϊ1��8��A�����������
�뻹ԭ��Fe2�������ʵ���֮��Ϊ1��8��A�����������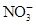 ����ԭ�õ���ԭ����
����ԭ�õ���ԭ����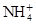 ��B����ȷ������1 mol
��B����ȷ������1 mol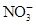 �μӻ�ԭ��Ӧ����ת��8 mol e����C����ȷ����������ԭ��Ӧ��������ӦΪFe2����e��=Fe3�������Ϊԭ�����Ϊ������Ӧ��D����ȷ
�μӻ�ԭ��Ӧ����ת��8 mol e����C����ȷ����������ԭ��Ӧ��������ӦΪFe2����e��=Fe3�������Ϊԭ�����Ϊ������Ӧ��D����ȷ
�����Ѷȣ�һ��
2������� I���ס���Ԫ�صĵ��ʺͻ�����Ӧ�ù㷺��
��1����Ԫ�ص�ԭ�ӽṹʾ��ͼ��______��
��2��������뽹̿��ʯӢɰ��ϣ��ڵ�¯�м��ȵ�1500�����ɰ��ף���ӦΪ��
2Ca3��PO4��2+6SiO2�T6CaSiO3+P4O10?10C+P4O10�TP4+10CO
ÿ����1mol?P4ʱ������______mol���ӷ���ת�ƣ�
��3����������ƣ�Na2S2O3���dz��õĻ�ԭ������ά����C����ѧʽC6H8O6����ˮ��Һ�м������I2��Һ��ʹά����C��ȫ������ʣ���I2��Na2S2O3��Һ�ζ����ɲⶨ��Һ��ά����C�ĺ����������ķ�ӦΪ��
C6H8O6+I2�TC6H6O6+2H++2I-?2S2O32-+I2�TS4O62-+2I-
��һ�������ijά����C��Һ�м���a?mol?L-1I2��ҺV1mL����ַ�Ӧ����Na2S2O3��Һ�ζ�ʣ���I2������b?mol?L-1Na2S2O3��ҺV2mL������Һ��ά����C�����ʵ�����______mol��
��4����������Һ�У�����أ�KIO3�����������ƿɷ������·�Ӧ��2IO3-+5SO32-+2H+�TI2+5SO42-+H2O
���ɵĵ�����õ�����Һ���飬���ݷ�Ӧ��Һ������ɫ�����ʱ���������÷�Ӧ�����ʣ�ijͬѧ���ʵ�������ʾ��
| 0.01mol?L-1
KIO3������Һ�������ۣ������/mL | 0.01mol?L-1
Na2SO3��Һ�����/mL | H2O�����
/mL | ʵ��
�¶�
/�� | ��Һ������ɫʱ����ʱ��/s
ʵ��1
5
V1
35
25
ʵ��2
5
5
40
25
ʵ��3
5
5
V2
0
|
��ʵ���Ŀ����______������V2=______mL
II��ϡ��Ԫ���DZ����ս����Դ���ҹ����̲�����������λ��
��5���棨Ce���ǵؿ��к�����ߵ�ϡ��Ԫ�أ��ڼ���������CeCl3����ˮ�⣬��ˮCeCl3���ü���CeCl3?6H2O��NH4Cl��������ķ������Ʊ�������NH4Cl��������______��
��6����ijǿ���Ի��ϡ����Һ�м���H2O2������pH��3��Ce3+ͨ�����з�Ӧ�γ�Ce��OH��4�������Է��룮��ɷ�Ӧ�����ӷ���ʽ��______Ce3++______H2O2+______H2O�T______Ce��OH��4��+______��
�ο��𰸣���1��P���ڵ�15��Ԫ�أ���ԭ�ӵĽṹʾ��ͼΪ

���ʴ�Ϊ��

��
��2��ÿ����1 mol P4ʱ��P��+5�۱��0�ۣ�����ת��Ϊ5��4 mol=20 mol��C���ϼ���0�۱��Ϊ+2�ۣ�����ת��Ϊ2��10 mol=20 mol���ʴ�Ϊ��20��
��3��I2��Һһ��������������Ʒ�Ӧ��һ������ά����C��Ӧ��n��Na2S2O3��=bV21000mol��
���䷴Ӧ�ĵⵥ��Ϊ bV22000mol����ά����C��Ӧ�ĵⵥ��Ϊ 2aV1-bV22000mol��
��ά����C�����ʵ����� 2aV1-bV22000=aV1-0.5bV21000��
�ʴ�Ϊ��2aV1-bV22000��
��4����ʵ��2���Կ������Һ�������Ϊ50mL��V1Ϊ10mL��V2Ϊ40mL��ʵ��1��ʵ��2��֪ʵ��Ŀ����̽���÷�Ӧ����������������ҺŨ�ȵĹ�ϵ��ʵ��2��ʵ��3��֪ʵ��Ŀ����̽���÷�Ӧ�������¶ȵĹ�ϵ��
�ʴ�Ϊ��Ŀ����̽���÷�Ӧ��������������Ũ�ȣ���Ӧ�¶ȵĹ�ϵ��V2=40?mL��
��5����Ŀ�и�����������������CeCl3����ˮ�⡱����֪NH4Cl�������ǿ϶�������ˮ��ģ�CeCl3ˮ�������HCl����֪NH4Cl�������Ƿֽ��HCl���壬����CeCl3ˮ�⣬
�ʴ�Ϊ���ֽ��HCl���壬����CeCl3��ˮ�⣻
��6���������⣺��ǿ���ԡ���۲췽��ʽ��֪ȱ����H+�����õ��ӵ�ʧ�غ��۲취�Ϳ�����ƽ����ʽΪ2Ce3++H2O2+6H2O�T2Ce��OH��4��+6H+��
�ʴ�Ϊ��2��1��6��2��6H+��
���������
�����Ѷȣ�һ��
3��ѡ���� ����Fe2����I����Br������Һ��ͨ��������������Һ�и������ӵ����ʵ����仯��ͼ��ʾ���й�˵������ȷ����
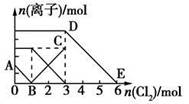
A���߶�BC����Fe3�����ʵ����ı仯���
B��ԭ�����Һ��n(FeBr2)��3 mol
C����ͨ��2 mol Cl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��
2Fe2����2I����2Cl2===2Fe3����I2��4Cl��
D��ԭ��Һ��n(Fe2��):n(I��):n(Br��)��3:1:2
�ο��𰸣�D
������������⿼���˻�ѧͼ��Ԫ�ػ���������ʡ�������ԭ��Ӧ����ѧ����ȣ����ڿ��鿼����ʶͼ������������������ԭ��˳��Br��<Fe2��<I�������ݻ�ѧͼ��Ӧԭ��֪���߶�AB����I�����ʵ����ı仯������߶�BC����Fe3�����ʵ����ı仯������߶�DE����Br�����ʵ����ı仯�����A����ȷ������ͼ������������������֪��ԭ��Һ��n(I��)��2 mol��n(Fe2��)��4 mol��n(Br��)��6 mol��n(Fe2��):n(I��):n(Br��)��2:1:3��D�����n(FeBr2)��3 mol��n(FeI2)��1 mol��B����ȷ����ͨ��2 mol Cl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��2Fe2����2I����2Cl2===2Fe3����I2��4Cl����C����ȷ��
�����Ѷȣ�һ��
4��ѡ���� �������ǿ�������·ֽ⣬���ɰ���������������ˮ����Ӧ�����ɵ���������ͻ�ԭ��������ʵ���֮���ǣ�?��
A��1:3
B��2:3
C��1:1
D��4:3
�ο��𰸣�B
���������3(NH4)2SO4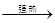 4NH3����3SO2����N2����6H2O
4NH3����3SO2����N2����6H2O
������ɵ���������N2�ͻ�ԭ����SO2�����ʵ���֮����1:3��ѡA��
�����Ѷȣ�һ��
5�������� (5��)����п��п�Ļ����14.6 g������Ũ��Ϊ1 mol/L������500 mL����ַ�Ӧ��������Һ��Zn2+�����ʵ���Ũ��Ϊ0.4 mol/L,��ԭ�����������п��п�����ʵ����������跴Ӧǰ����Һ������䣩
�ο��𰸣�(5��)n(Zn)="n" (ZnO)="0.1" mol
�����������
�����Ѷȣ���