1��ʵ���� ijУ����С��Ϊ��̽��ͭ��ϡ���ᷴӦ������������Ҫ��NO�����������ʵ�飬װ����ͼ��ʾ(����װ�ú̶�װ�þ�����ȥ)��ͼ��KΪֹˮ��(���ڹر�״̬)��F��һ��յ�ע������
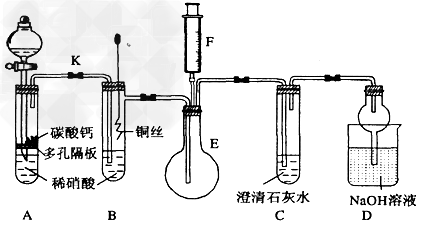
��ش��й����⣺
(1)?���װ��A��Ŀ����___________________��Ϊ�ﵽ��Ŀ�ģ�Ӧ���еIJ����Ǵ�K���Ҵ�Һ©����������װ��C�в���______________ʱ���ر�K��
(2)?�����(1)�еġ���������װ��B��ͭ˿����ϡ���ᣬ����֮���۲쵽װ��B�е�������______________�� B�з�Ӧ�����ӷ���ʽΪ��________________________��
(3)?װ��E��F��������________________��Ϊʵ�ִ����ã������������_____________________________��
(4)?װ��D�����������ն���ĵ��������ֹ��Ⱦ����������________________�Ĺ��ܡ�
�ο��𰸣�(1)�������ɵĶ�����̼������װ���ڵĿ����Ͼ�������NO��������Ӧ���ɶ����������������Ĺ۲�������ţ���ɫ����
(2)ͭ˿����������ݣ�ϡ����Һ������Ϊ��ɫ����Һ��Ϊ��ɫ��3Cu+8H++2NO3-=3Cu2++
2NO��+4H2O
(3)��֤��ɫ����ΪNO����ע����F�еĿ�������E�л�E�е���ɫ�������뵽ע������
(4)��ֹ��Һ����
���������
�����Ѷȣ�һ��
2������� ����ǻ�ѧѧϰ�г��õķ���֮һ����֪�����ܰ��������� Fe ( NO3)3��������������ʱ�������� Fe ( NO3 ) 2��ijͬѧ�ܴ����������һ�����ƵĹ۵㣺���������۷�Ӧ���� C12����ʱ���� FeC13 , �����۹���ʱ������ FeCl2��Ϊ��֤�ù۵��Ƿ���ȷ����ͬѧ��һ��ϸ�Ĵ���˿�ֱ��������������� C12�е�ȼ��ȡ����������ﲢ�ֱ���Ϊ A��B ��Ȼ��ͨ��ʵ��ȷ����ɷ֡�̽���������£�
( 1 ��������裺 A �� FeCl3, B �� FeCl 2��
( 2 �����ʵ�鷽�����ֱ�ȡ A��B ����Һ����������ʵ�飬��ʵ��������ͬ������д�±��е���Ӧ�ո�

( 3 ����������ʵ����ۣ�д�� C12�����ۼ���ʱ������Ӧ�Ļ�ѧ����ʽ��
_________________________________________________________________��
( 4 ��Ϊ��һ��̽�� FeC13��Һ�����ʣ��������� A ��Һ��������һЩʵ�飬�������Դ������____________________��
A���� A ��Һ�����ˮ�У����������ȵõ����ɫҺ�壬��Һ���ܲ������������
B���� A ��Һ�м����������ۣ������ܽ⣬��Һ��ɫ����
C���� A ��Һ�еμ� Na OH Ũ��Һ�����ֺ��ɫ����
D���� A ��Һ�������ɲ����գ��õ� FeC13����
( 5 ��ʵ��Ӧ�ã�
FeCl3��Һ����ӡˢ��·ͭ�帯ʴ������ʴ��ķ�Һ�к��� FeC13��FeCl2��CuCl2��ij�о���ѧϰС���ͬѧ����������ִӷ�Һ�л��� Cu�ķ�����
����1�����Һ�м��˹��������ۣ���ַ�Ӧ���ˡ������������м������������ᣬ��ַ����ٹ��˼��õ�ͭ������1 ���漰�����������ӵ���������ǿ������˳��Ϊ��
_____________________________________��
����2 ���ڷ�Һ�м������������������Һ�� pH =" 1" ����ͭ��ʯī���缫���е�⡣���۲쵽���������������ݲ���ʱ����ֹͣ��⣬��ʱҪ���յ� Cu ��ȫ������������ 2 ��ͭ��_________�����������ĵ缫��ӦΪ�����ж���缫��Ӧ���밴�շ�Ӧ�������Ⱥ�˳��ȫ��д����___________________________________________________
���� 2 �ڵ缫��ֱ�ӻ���ͭ�������ϱȷ��� 1 ��㣬������ 2 Ҳ�в���֮������Ҫ����Ϊ��_____________________________________________________��
�ο��𰸣���2����Һ���ɫ��1�֣� FeCl2 ( 1 �֣� ( 3 ) 2Feʮ3Cl2 2FeCl3 ( l �֣�
2FeCl3 ( l �֣�
( 4 ) BD (2�֣� ( 5 ������ 1 : Fe3+ ��Cu2+ > H + > Fe2+ ( l �֣�
���� 2 ������ l �֣�2Fe 3+��2eһ��2Fe2+ ;
Cu2+ + 2eһ��Cu ( l �֣�;
2H + + 2eһ��H2���� ( l �֣�
����Ⱦ������ C12������ l �֣���ʹ���˵��װ�ã��ɱ��ϸߵȡ��� l �֣�
���������Fe3+��SCNһ���ɫ�� Fe2+��ʹ KMnO4��Һ��ɫ�� FeC13��Һ�������ۣ�����������ԭΪ����������ɫ��dz�� FeC13��Һ�����������õ����������������� ( 5 �����Һ�м��˹��������ۣ��������Ⱥ����������ӷ�Ӧ������ת��Ϊ���������ӣ�Ȼ���ͭ���ӷ�Ӧ���ټ������ᣬ������������۷�Ӧ���ɶ��������ӣ��ɴ�֪�������ӵ���������ǿ������˳��ΪFe3+ ��Cu2+ > H+ ��Fe2+������ 2 ����ͭ���������缫�ϵķ�ӦΪ2Fe3+��2eһ��2Fe2+��Ȼ�� Cu2+��2eһ��Cu , 2H+ʮ2eһ��H 2�� , ����֮�������������������Ⱦ�������Ĵ����ĵ��ܵȡ�
�����Ѷȣ�һ��
3��ʵ���� ��15�֣��ӹ�������A�������Է������¿�ͼ��ʾ��һϵ�б仯��

(1)��ʵ���ң�����C�ļ��鷽����??����? (2)�����ڵ������� ?���ò�����ʹ�õIJ���������?��
(3)д�����з�Ӧ�����ӷ���ʽ��������
��Ӧ�� ??��
��Ӧ�� ??����
(4)ʵ���ж��������I�������գ�������Ⱦ��������ͼ��ʵ������NaOH��������I��װ�ã�Ϊ��ֹ������������������װ����??(�����)��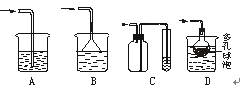
�ο��𰸣�

�����������
�����Ѷȣ���
4������� ij�о���ѧϰС�齫ʵ�����Ʊ�������̼���巴Ӧ��ķ�����д�����Ŀ������ȡ���Ը����CaCl2���õ���������ǶԹ���ijɷֽ���������̽����
[�������]
����һ��ֻ��CaCl2
�������CaCl2��CaCO3
��������CaCl2��HCl
ͨ�����ۣ������Ϊ������������������������______��
[ʵ��̽��]
| ���� | ���� | ����
����һ
______ |
���������
�����

______
|
��1��д���йط�Ӧ�Ļ�ѧ����ʽ��______
��2��ʵ�������ͬѧ�Ǹ��ݸ��ֽⷴӦ�������������ܽ���õ�CaCl2�IJ�ͬ;�����磺
��Ca��OH��2+YCla��CaCl2+Z������ôZ������______����һ�����ʵĻ�ѧʽ���ɣ���
��CaXm+2YClb��CaCl2+H2O����YClb������______�����ʣ�
��3��ͬѧ��������ȵķ�����CaCl2���ܾ��еĻ�ѧ���ʽ�����̽�����ܽ�����������������е�______������Ӧ�����ţ���
��HNO3?��AgNO3?��Na2CO3?��Fe��OH��3?��Mg?��BaCO3��
�ο��𰸣�[�������]�õ���������ǶԹ���ijɷֽ�����̽���������IJ����У�������������������������CaCl2�ǹ��壬�Ȼ�����������ˮ�����ᣬ������Һ�壬
�ʴ�Ϊ��CaCl2�ǹ��壬������Һ�壨CaCl2�ǹ��塢������Һ�塢�����ӷ����������ɣ���
[ʵ��̽��]̽�������ǹ��壬���������е�HCl�����壻����̼��Ʋ�����ˮ����Ʒ����ˮ�����岿���ܽ⣬��ϡ���ᷴӦ������ð���������ж�̼����Ƿ���ڣ��ʴ�Ϊ��
��������ʵ����۲���һ���岿���ܽⲽ��������ܽ⣬�������ݣ�1��̼��ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼����ƽ��ķ�ӦΪCaCO3+2HCl=CaCl2+CO2��+H2O���ʴ�Ϊ��CaCO3+2HCl=CaCl2+CO2��+H2O��
��2�����ݸ��ֽⷴӦ�������������ܽ���õ�CaCl2�IJ�ͬ;����������η�Ӧ�����¼�����Σ����Z������Cu��OH��2��Fe��OH��3��Mg��OH��2��Zn��OH��2��Al��OH��3��Fe��OH��2�������Լ������������������ᷴӦ�����κ�ˮ����ˡ�YCln�������ᣬ
�ʴ�Ϊ����Cu��OH��2[Fe��OH��3��Mg��OH��2��Zn��OH��2��Al��OH��3��Fe��OH��2�������Լ���
��3�����Ȼ��ƺ������Ӧ���ٲ����ϣ�
��AgNO3 �Ȼ��ƺ���������Ӧ�����Ȼ����������ʢڷ��ϣ�
��Na2CO3�� �Ȼ��Ʒ�Ӧ����̼��Ƴ������ʢ۷��ϣ�
��Fe��OH��3 ���Ȼ��Ʋ���Ӧ���ʢܲ����ϣ�
��Mg�����Ȼ��Ʒ�Ӧ���ʢݲ����ϣ�
��BaCO3�����Ȼ��Ʒ�Ӧ���ʢ����ϣ�
�ʴ�Ϊ���ڢۣ�
���������
�����Ѷȣ�һ��
5������� ij��ѧ����С�����������ͼ������̨������ȥ����ʾ��ʵ��װ�ã�������������ʵ�顣ͼ���ü�ͷ��ʾ��������A��ʾһ�ִ�������������壬B��ʾ��һ�����塣��Ӧ����һ��ʱ���װ�ü����к���ɫ�������ɡ�ʵ�������õ�ҩƷ�����ֻ�ܴ�����������ѡȡ��N a2CO3��NaHCO3��MnO2��Na2O2��NaCl����ˮCaCl2��NH4HCO3����ʯ�ҵȹ����H2O2������ˮ��
a2CO3��NaHCO3��MnO2��Na2O2��NaCl����ˮCaCl2��NH4HCO3����ʯ�ҵȹ����H2O2������ˮ��
����ͼ��װ�úͷ�Ӧ������ش�
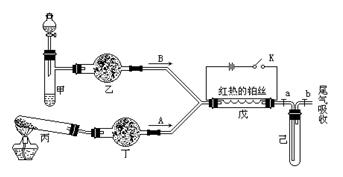
��1�����з�����Ӧ�Ļ�ѧ����ʽΪ?��
��2�����еĸ����Ӧѡ?����ѡ��һ�ָ������������?��
��3�����з�����Ӧ�Ļ�ѧ����ʽΪ? ?��
?��
��4�����з�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ?���˷�Ӧ�ǣ����ȡ����ȣ�?��Ӧ�����ܷ�����ʲô�������֤������ж�?��
�ο��𰸣���1��NH4HCO3 NH3����CO2����H2O����2�֣�
NH3����CO2����H2O����2�֣�
��2����ʯ�ң�1�֣�����ˮCaCl2ֻ����ˮ����������CO2����NH3Ҫ����ˮCaCl2��Ӧ�� 1�֣�
��3��2H2O2 2H2O��O2������2Na2O2��2H2O
2H2O��O2������2Na2O2��2H2O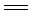 4NaOH��O2������2�֣�
4NaOH��O2������2�֣�
��4��4NH3��5O2 4NO��6H2O��2�֣������ȣ�1�֣�����Ӧ��ʼ��Ͽ����K����˿�ܼ������ֺ��ȣ�1�֣���
4NO��6H2O��2�֣������ȣ�1�֣�����Ӧ��ʼ��Ͽ����K����˿�ܼ������ֺ��ȣ�1�֣���
�����������
�����Ѷȣ�һ��