| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《物质的组成》在线测试(2019年最新版)(六)
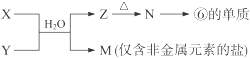 X溶液与Y溶液反应的离子方程式?,? M中阳离子的鉴定方法?。 参考答案:(1)Na (2)第三周期第ⅣA族 本题解析:(1)对于电子层数相同的元素来说,原子序数越大,原子半径越小;对于电子层数不同的元素来说,原子核外的电子层数越多,原子半径越大。所以在题目已知的元素中,原子半径最大的是Na. (2)地壳中含量居于第二位的元素Si在周期表中的位置是第三周期第ⅣA族。(3)①是H;④是O;⑤是Na.在这三种元素中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式为 本题难度:一般 5、选择题 已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物在常温下均呈气态,在周期表中Z与W左右相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同。请回答下列问题: 参考答案:(共12分)(1)1s22s22p63s23p4(2分)?(2)?极性键、离子键、配位键(2分)?(3)三角锥形;sp3 ;高(每空2分)? 本题解析:X与Y、Z、W所形成的常见化合物在常温下均呈气态,,多为氢化物,则X为H元素,Y的最高价氧化物对应的水化物与其氢化物反应生成盐,则Y应为N元素,形成的化合物NH4NO3,Y的核电荷数为7,与W的最外层电子数相同,则W可能为F,也可能为Cl元素,如W为F元素,则Z为O元素,Z对应的氢化物为H2O,在常温下为液体,不成立,所以W为Cl元素,Z为S元素。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《与量有关的.. | |