1、填空题 (16分)随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,CO2的排放量也要大幅减少。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ・mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
③CH4(g)+2NO2 (g)= N2(g) + CO2(g)+2H2O(g) △H3=-867kJ・mol-1
则△H2= 。
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。
(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为C(s) + H2O(g)  CO(g) + H2(g)
CO(g) + H2(g)
①该反应的化学平衡常数表达式为:K= 。
②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应: CO(g) + H2O(g)  CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol・L-1,则CO的转化率为_________,800℃时该反应的平衡常数为_________。
CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol・L-1,则CO的转化率为_________,800℃时该反应的平衡常数为_________。
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应_______________________________________。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是: ___________。
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g) CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
如图所示。由下图可以得出的结论是(写两条):_____________________、___________________。

参考答案:Ⅰ.-1160KJ/mol (2分) Ⅱ.(1) ①K=[c(CO)?c(H2)] /c(H2O) (2分)②50%(2分) 0.6(2分) (2) ①SO2+2H2O+I2=4H++SO42-+2I- ②对于平衡:2HI(g)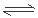 I2(g)+H2(g),分离出H2,实质是降低了生成物的浓度,使平衡向正反应方向移动(2分)。Ⅲ.其它条件不变时,100―250℃之间,温度升高,催化剂的催化效率升高;其它条件不变时,100―250℃之间,温度升高,乙酸的生成速率加快;其它条件不变时,250℃―300℃之间,温度升高,催化剂的催化效率降低;250℃―300℃之间,温度升高,乙酸的生成速率减慢;300℃―400℃之间,温度升高,催化剂的催化效率变化不大;300℃―400℃之间,温度升高,乙酸的生成速率加快;(4分以上6条写2条即可,其它合理答案均可)
I2(g)+H2(g),分离出H2,实质是降低了生成物的浓度,使平衡向正反应方向移动(2分)。Ⅲ.其它条件不变时,100―250℃之间,温度升高,催化剂的催化效率升高;其它条件不变时,100―250℃之间,温度升高,乙酸的生成速率加快;其它条件不变时,250℃―300℃之间,温度升高,催化剂的催化效率降低;250℃―300℃之间,温度升高,乙酸的生成速率减慢;300℃―400℃之间,温度升高,催化剂的催化效率变化不大;300℃―400℃之间,温度升高,乙酸的生成速率加快;(4分以上6条写2条即可,其它合理答案均可)
本题解析:Ⅰ.③×2-①,整理可得:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=2△H3-△H1=2×(-867kJ/mol)+574kJ/mol=-1160KJ/mol;Ⅱ.(1)①反应为C(s) + H2O(g)  CO(g) + H2(g) 的化学平衡常数表达式为:
CO(g) + H2(g) 的化学平衡常数表达式为: ;②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应:[ CO(g) + H2O(g)
;②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应:[ CO(g) + H2O(g)  CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol・L-1,则CO的转化率为
CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol・L-1,则CO的转化率为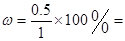 50%,则平衡时各种物质的浓度分别是:c(CO)=0.5mol/L;c(H2O)="2." 5mol/L;c(CO2)=0.5mol/L;c(H2)=1.5mol/L;所以800℃时该反应的平衡常数为
50%,则平衡时各种物质的浓度分别是:c(CO)=0.5mol/L;c(H2O)="2." 5mol/L;c(CO2)=0.5mol/L;c(H2)=1.5mol/L;所以800℃时该反应的平衡常数为 ;(2)①在反应器中SO2、I2、H2O发生氧化还原反应产生硫酸和氢碘酸,用离子方程式表示反应器中发生的反应是SO2+2H2O+I2=4H++SO42-+2I-;②碘化氢分解反应是可逆反应;当从反应体系分离出H2,实质是降低了生成物的浓度,根据平衡移动原理:降低生成物的浓度,平衡正向移动,可以使反应得到的I2再回到反应器中促进SO2的转化吸收;Ⅲ.根据图像可知其它条件不变时,100―250℃之间,温度升高,催化剂的催化效率升高;其它条件不变时,100―250℃之间,温度升高,乙酸的生成速率加快;其它条件不变时,250℃―300℃之间,温度升高,催化剂的催化效率降低;250℃―300℃之间,温度升高,乙酸的生成速率减慢;300℃―400℃之间,温度升高,催化剂的催化效率变化不大;300℃―400℃之间,温度升高,乙酸的生成速率加快;
;(2)①在反应器中SO2、I2、H2O发生氧化还原反应产生硫酸和氢碘酸,用离子方程式表示反应器中发生的反应是SO2+2H2O+I2=4H++SO42-+2I-;②碘化氢分解反应是可逆反应;当从反应体系分离出H2,实质是降低了生成物的浓度,根据平衡移动原理:降低生成物的浓度,平衡正向移动,可以使反应得到的I2再回到反应器中促进SO2的转化吸收;Ⅲ.根据图像可知其它条件不变时,100―250℃之间,温度升高,催化剂的催化效率升高;其它条件不变时,100―250℃之间,温度升高,乙酸的生成速率加快;其它条件不变时,250℃―300℃之间,温度升高,催化剂的催化效率降低;250℃―300℃之间,温度升高,乙酸的生成速率减慢;300℃―400℃之间,温度升高,催化剂的催化效率变化不大;300℃―400℃之间,温度升高,乙酸的生成速率加快;
考点:考查盖斯定律的应用、化学平衡常数和物质的平衡转化率的计算、外界条件对平衡的影响、图像法在化学反应平衡移动中的作用、离子方程式的书写的知识。
本题难度:困难
2、填空题 (12分)(1)环境专家认为可以用金属铝将水体中的NO3-转化为N2,从而消除污染。该反应中涉及的微粒有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将这些微粒中除NO3-以外的微粒填入以下空格内(不用配平)。

该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应是4Al +3O2+6H2O ="4" Al(OH)3。电池正极的电极反应式是 ;消耗13.5 g Al时转移_________mole-。
(3) 铝与某些金属氧化物在高温下的反应称为铝热反应,可用于冶炼高熔点的金属。
已知:4Al(s) +3O2(g) = 2Al2O3(s)△H = -2830 kJ/mol
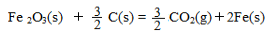 △H = +230 kJ/mol
△H = +230 kJ/mol
C(s)+O2(g) = CO2(g) △H = -390 kJ/mol
铝与氧化铁发生铝热反应的热化学方程式是 ,铝热反应属于______(填字母)反应。
a.氧化还原 b.复分解 c.置换
参考答案:(1)NO3- + Al +H2O→ Al(OH)3 + N2 + OH-(2分) 5∶3
(2)O2+4e-+2H2O=4OH- 1.5
(3)2 Al(s) + Fe2O3 (s)= 2 Fe(s) +Al2O3 (s) △H = - 600 kJ/mol a c
本题解析:(1)根据金属铝将水体中的NO3-转化为N2,可知Al为还原剂,则Al(OH)3为氧化产物,再根据电荷守恒和原子守恒可得:NO3- + Al +H2O→ Al(OH)3 + N2 + OH-;Al元素被氧化,N元素被还原,则被氧化与被还原的元素的物质的量分别为x、y,由电子守恒可知,x×(3-0)=y×(5-0),解得x:y=5:3,所以被氧化与被还原的元素的物质的量之比为5∶3。
(2)由电池总反应4Al+3O2+6H2O=4Al(OH)3可知,Al作负极,氧气在正极上得电子发生还原反应,正极反应为2H2O+O2+4e-=4OH-;Al元素由0价升高为+3价,则 Al~3e?,所以消耗13.5 g Al时转移电子:13.5g÷27g/mol×3=1.5mol。
(3)首先写出化学方程式并注明各物质的状态,然后根据盖斯定律求出?H,?H="1/2" ?H1+?H2
本题难度:困难
3、选择题 下列说法正确的是( )
A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量
B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据
C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态
D.凡是化合反应都是放热反应,分解反应都是吸热反应
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列中和反应热化学方程式可用:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1来表示的是( ? )
A.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H=-Q1?kJ?mol-1
B.
 H2SO4(浓)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l);△H=-Q2?kJ?mol-1
H2SO4(浓)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l);△H=-Q2?kJ?mol-1
C.HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l);△H=-Q3?kJ?mol-1
D.
 H2SO4?(aq)+
H2SO4?(aq)+ Ba(OH)2(aq)=
Ba(OH)2(aq)= BaSO4?(s)+H2O(l);△H=-Q4?kJ?mol-1
BaSO4?(s)+H2O(l);△H=-Q4?kJ?mol-1
参考答案:C
本题解析:
本题难度:一般
5、填空题 (10分)工业制氢气的一个重要反应是:CO(g)+H2O(g)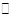 CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知在25。C时:
①C(石墨)+1/2O2(g)=CO(g) △H1=-111kJ・mol-1
②C(石墨)+O2(g)=CO2(g) △H2=-394kJ・mol-1
③H2(g)+1/2O2(g)=H2O(g) △H3=-242kJ・mol-1
则反应CO(g)+H2O(g) ="==" CO2(g)+H2(g)的反应热△H=___________.
(2)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:

①以下反应能说明CO(g)+H2O(g) CO2(g)+H2(g)达到平衡状态的是_________
CO2(g)+H2(g)达到平衡状态的是_________
A.容器中CO的含量保持不变
B.容器中CO2浓度与CO浓度相等
C.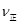 (CO)=
(CO)=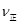 (H2O)
(H2O)
D.容器中混合气体的平均相对分子质量保持不变
 (CO)=_____;
(CO)=_____;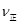 ___________
___________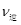 (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
(填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)