1、选择题 下列关于氯水的叙述,正确的是
A.新制氯水中只含有Cl2、H2O和H+三种微粒
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后酸性减弱
参考答案:B
本题解析:A、氯气溶于水即得到氯水,在新制氯水中含有Cl2、H2O、HClO、Cl-、ClO-、OH-和H+六种微粒,A不正确;B、新制氯水显酸性,同时还具有强氧化性,因此新制氯水可使蓝色石蕊试纸先变红后褪色,B正确;C、氯水中的次氯酸不稳定,受热易分解生成氯化氢和氧气,因此光照氯水有气泡逸出,该气体是氧气,C不正确;D、氯水中的次氯酸不稳定,受热易分解生成氯化氢和氧气,因此氯水放置数天后酸性增强,D不正确,答案选B。
本题难度:一般
2、简答题 (12分)空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。
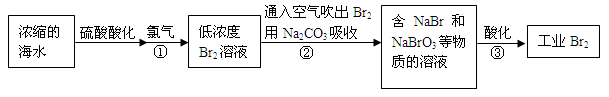
(1)NaBr的电子式是?。
(2)反应①是将Br―转化为Br2,反应①的离子方程式是?。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是?。?
(4)反应②的化学方程式是?。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是?mol。?
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中?(填字母)。
a.通入HBrb.加入NaBr溶液?c.加入Na2CO3溶液?d.加入Na2SO3溶液
参考答案:(12分,每空2分)
(1) 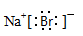
(2)Cl2+2Br― Br2+2Cl―(物质1分,配平1分)
Br2+2Cl―(物质1分,配平1分)
(3)富集溴
(4)3Br2+3Na2CO3 5NaBr+3CO2+NaBrO3 (物质1分,配平1分)
5NaBr+3CO2+NaBrO3 (物质1分,配平1分)
?(5)5?
(6)b
本题解析:(1)NaBr是离子化合物,其电子式为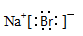
(2)反应①是氯气与溴离子反应生成溴单质和氯离子,离子方程式为Cl2+2Br― Br2+2Cl―
Br2+2Cl―
(3)溴易挥发,碳酸钠溶液显碱性,与吹出的溴反应,减少损失,达到富集溴的目的;
(4)反应②的反应物是溴与碳酸钠,根据题目所给信息,生成物是NaBr和NaBrO3及二氧化碳,化学方程式为3Br2+3Na2CO3 5NaBr+3CO2+NaBrO3
5NaBr+3CO2+NaBrO3
(5)反应③是5Br-+H++BrO3-= 3Br2+H2O,则每生成3 mol Br2,转移电子的物质的量是5mol;
(6)a、氯气不与溴化氢反应,不能除去,错误;b、氯气与溴化钠反应生成溴和氯化钠,正确;c、氯气与溴单质都能与碳酸钠溶液反应,错误;d、氯气与溴都能氧化亚硫酸钠,错误,答案选b。
本题难度:一般
3、选择题 下列对氯气的性质描述错误的有( )
A.密度比空气大
B.无色,有剌激性气味
C.能使品红溶液褪色
D.可与消石灰反应制漂白粉
参考答案:A.同温同压下,根据ρ=MVm知,密度和相对分子质量成正比,氯气的相对分子质量大于空气,所以氯气的密度大于空气,故A正确;
B.氯气是黄绿色有刺激性气味的有毒气体,故B错误;
C.氯气和水反应生成次氯酸,次氯酸有强氧化性,能漂白品红溶液,故C正确;
D.氯气和消石灰反应生成次氯酸钙,次氯酸钙具有漂白性,是漂白粉的有效成分,故D正确;
故选B.
本题解析:
本题难度:简单
4、选择题 在通常状况下呈黄绿色的气体是( )
A.N2
B.H2
C.Cl2
D.CO2
参考答案:N2、H2和CO2都为无色气体,Cl2为黄绿色的气体.
故选:C.
本题解析:
本题难度:一般
5、选择题 在NaCl溶液中滴加AgNO3溶液,再滴加KI溶液,下列描述正确的是:
A.先产生白色沉淀后产生黄色沉淀
B.先产生白色沉淀后无明显现象
C.先产生黄色沉淀后产生白色沉淀
D.实验证明AgCl溶解度小于AgI溶解度。
参考答案:A
本题解析:考查溶解平衡知识。
首先Cl-+Ag+=AgCl↓,但由于AgI较AgCl更难溶,白色沉淀AgCl会逐渐转化为黄色沉淀AgI:AgCl+I-=AgI+Cl-,故现象为先产生白色沉淀后产生黄色沉淀,选A
本题难度:一般