1、选择题 下列叙述正确的是
A.标准状况下,l mol任何物质的体积均为22.4 L
B.CH4的摩尔质量为16 g
C.1mol H2O的质量为18 g?mol-1
D.3.01×l023个SO2分子的质量为32 g
参考答案:D
本题解析:A、标准状况下,l mol任何气体的体积均为22.4 L,错误;B、摩尔质量的单位是g?mol-1 ,CH4的摩尔质量应为16 g?mol-1,错误;C、1mol H2O的质量应为18 g,错误;D、3.01×l023个SO2分子的物质的量为0.5mol,质量为32 g,正确。
本题难度:一般
2、简答题 某同学用18mol/L的浓硫酸配制200mL?0.9mol/L的稀硫酸,并进行有关实验.请回答下列问题:
(1)需要量取浓硫酸______mL.
(2)配制该稀硫酸时使用的仪器除量筒、烧杯、200mL容量瓶外,还必须用到的仪器有______、______等.
(3)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是______
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度线改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响
(4)在配制过程中,下列因素对所配制的稀硫酸的物质的量浓度有何影响?
若容量瓶未干燥即用来配制溶液,则所得溶液浓度______0.9mol?L-1(填“大于”、“等于”或“小于”,下同);若定容时俯视刻度线,则所得溶液浓度______0.9mol?L-1.
(5)取所配制的稀硫酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.448L,则参加反应的锌的质量为______g;设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为______mol/L.
参考答案:(1)根据稀释定律,稀释前后溶质的物质的量不变,来计算浓浓硫酸的体积,设浓硫酸的体积为xmL,
则xmL×18mol/L=200mL×0.9mol/L,解得:x=10.0,所以应量取的浓硫酸体积是10.0mL.
故答案为:10.0.
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却至室温后转移到200mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀.
所以需要的仪器为:玻璃棒、烧杯、胶头滴管、量筒、200mL容量瓶,
故答案为:胶头滴管;玻璃棒.
(3)容量瓶的瓶颈改粗,会降低容量瓶的精确度.
故选:B.
(4)若容量瓶未干燥即用来配制溶液,最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
若定容时俯视刻度线,导致溶液体积偏小,所配溶液浓度偏大.
故答案为:等于;大于.
(5)Zn+H2SO4=ZnSO4+H2↑
?1mol?1mol? 22.4L
?x? y? 0.448L
所以x=0.448L22.4L×1mol=0.02mol.
? y=x=0.02mol.
所以参加反应锌的质量为0.02mol×65g/mol=1.3g.
氢离子浓度变化量为△c(H+)=0.02mol×20.1L=0.4mol/L.
所以反应后溶液中的氢离子的物质的量浓度为2×0.9mol/L-0.4mol/L=1.4mol/L.
故答案为:1.3g;1.4mol/L.
本题解析:
本题难度:一般
3、选择题 有0.4 g铁的氧化物,用足量的CO在高温下将其还原,把生成的CO2全部通入足量澄清石灰水中,得到0.75 g沉淀。这种铁的氧化物的化学式是(?)
A.FeO
B.Fe2O3
C.Fe3O4
D.FeO和Fe2O3
参考答案:B
本题解析:CO和铁的氧化物反应时,氧化物中的一个O原子对应一个CO2分子,每一个CO2分子对应一个CaCO3,所以有下列的关系式,假设0.4 g该氧化物中含x g O原子。
O ~ CO2 ~ CaCO3
16?100
x g?0.75 g
解得x=0.12
N(Fe)∶N(O)=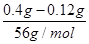 ∶
∶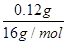 =2∶3。
=2∶3。
故此氧化物的化学式为Fe2O3。
本题难度:一般
4、选择题 设阿伏加德常数为NA。则下列说法正确的是
A.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
B.标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA
C.常温常压下,18g H2O中含有的电子数为3NA
D.常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA