|
�߿���ѧ֪ʶ����ɡ����ʵ���ɡ�����ǿ����ϰ��2019�����°棩(��)
2019-05-30 02:48:30
�� �� �� ��
|
1��ѡ���� �����и������ʵıȽϣ���ȷ���ǣ�������
�����ԣ�HClO4>HBrO4>HIO4?�����ӻ�ԭ�ԣ�S2->Cl->Br ->I-?�۷е㣺HF��HCl��HBr>HI
�ܽ����ԣ�K>Na>Mg>Al?����̬�⻯���ȶ��ԣ�HF��HCl��H2S?�ް뾶��O2->Na+>Na>Cl
A���٢ڢ�
B���ڢۢ�
C���٢ܢ�
D���٢ڢۢܢݢ�
�ο��𰸣�C
����������ٸ���ͬ����Ԫ�����ʵݱ�����жϣ��ǽ����ԣ�Cl��Br��I�����������ˮ��������ԣ�HClO4>HBrO4>HIO4����ȷ���ڸ��ݷǽ����Ի˳���жϣ��ǽ����ԣ�Cl>Br>I��S�����ӻ�ԭ�ԣ�S2->I- >Br - >Cl-��������ɺͽṹ���Ƶķ��Ӿ��壬��Է�������Խ�е�Խ�ߣ�HF���Ӽ����������е㷴���ĸߣ��ʷе㣺HF>HI��HBr��HCl�����ܸ���ͬ����Ԫ���������ҽ�����������ͬ����Ԫ�����ϵ��½�������ǿ֪�������ԣ�K>Na>Mg>Al����ȷ���ݸ��ݷǽ����Ի˳���жϣ��ǽ����ԣ�F��Cl��S ����̬�⻯���ȶ��ԣ�HF��HCl��H2S����ȷ���ް뾶��Na>Cl> O2->Na+������ѡC��
�����Ѷȣ�һ��
2������� ��8�֣�����Ԫ�ص�ԭ�ӵ��Ӳ�ṹ���£�
A��1s22s1��
B��1s22s22p4��
C��1s22s22p6��
D��1s22s22p63s23p2
| E��[Ar]3d104s1��
[��Ԫ�ط�������]
��1��Ԫ�صĵ�һ��������������?��
��2�����ڹ���Ԫ�ص���?��??��
��3��Ԫ�صĵ縺��������?��
��4������Ԫ��֮�����γ�X2Y�ͻ�����Ļ�ѧʽ��?����?��
�ο��𰸣���1��Ne?��2��Cu?��3��B?��4��Li2O? Cu2O
����������������и�����Ԫ��ԭ�ӵ��Ӳ�ṹ���Ƴ���A��LiԪ�أ� B��OԪ�أ� C��NeԪ�أ� D��SiԪ�أ� E��CuԪ�ء�C��ԭ�ӽṹ�ȶ�����ʧ���ӣ����һ���������E��d�������s�����Ϊ1 ������ds���ǹ���Ԫ�ء����õ��ӵ���O���縺�����O��������Ӳ㻹��2�����Ӳų����ģ������γ�Li2O��Cu2O�ȡ�
���������ڼ��⡣
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ����(����)
A��SiH4��CH4�ȶ�
B��O2���뾶��F����С
C��P��As���ڵڢ�A��Ԫ�أ�H3PO4���Ա�H3AsO4����
D��Na��Rb���ڵڢ�A��Ԫ�أ�Rbʧ����������Na��ǿ
�ο��𰸣�D
���������̼�ķǽ�����ǿ�ڹ�ģ����Լ����SiH4�ȶ���A����ȷ����������Ų���ͬ�����������뾶��ԭ���������������С��B����ȷ��ͬ�������϶��·ǽ���������������������ˮ�����������������C����ȷ��ͬ�������϶��½���������ǿ��������ȷ�Ĵ���D��
�����Ѷȣ�һ��
4������� ���ڱ���ǰ20�ż���Ԫ�أ��������Ϣ���£����ԭ�Ӱ뾶Ϊ0.089nm����
Ԫ�ش���
| A
| B
| C
| D
| E
| ԭ�Ӱ뾶/nm
| 0.075
| 0.143
| 0.102
| 0.099
| 0.074
| ��Ҫ���ϼ�
| +5����3
| +3
| +6����2
| ��1
| ��2
|
Fԭ���������ӣ�G�ڵؿ��к����ӵڶ�λ��HԪ����ɫ��Ӧ����ɫ��
��ش��������⣺
��1��B��ԭ�ӽṹʾ��ͼΪ?��
��2��F2C��F2E���ֻ������У��е�ϸߵ���?���ѧʽ����ԭ����?��
��3���õ���ʽ��ʾ������AF3���γɹ���?��
��4��G�ĵ�������H������������ˮ������Һ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ?��
��5��CE2��ʹ���Ը��������Һ��ɫ����Mn2+���ɣ���д���䷴Ӧ�����ӷ���ʽ?
?��
��6����2L�ܱ������У�һ���¶��£���˵����Ӧ2AE��g��+E2��g��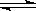 2AE2��g���Ѵﵽƽ��״̬����?������ţ� 2AE2��g���Ѵﵽƽ��״̬����?������ţ�
a. 2V�棨AE��=V����E2��
b.������ѹǿ���ֲ���
c. �������ܶȱ��ֲ���
d. ����ֵ����ʵ���Ũ�����
e. ��������ƽ����Է����������ٸı�
��7��ijͬѧ�������Gͬ��Ķ�����Ԫ�ص���ͼ��⻯��Ϊȼ�ϵĵ�أ��������Һ��HEF�� ��õ�صĸ����ĵ缫��ӦʽΪ?��
�ο��𰸣���14�֣���1��?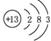 ��2�֣� ��2�֣�
��2��? H2O?��ˮ���Ӽ����γ���� (������������Ҳ��)?����1�֣�
��3��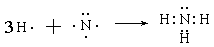 ?��2�֣� ?��2�֣�
��4��Si + H2O + 2KOH��K2SiO3 + 2H2��? (2��)
��5��5SO2 + 2MnO4�� + 2H2O��2Mn2+ + 5SO42�� + 4H+?(2��)
��6��be? (2��)?��7��CH4��10OH���D8e����CO32����7H2O?(2��)
�������������Ԫ�ص���Ҫ���ϼۺ�ԭ�Ӱ뾶��֪��A��NԪ�أ�B��AlԪ�أ�C��S���ڣ�D����Ԫ�أ�E����Ԫ�ء�Fԭ���������ӣ�����F����Ԫ�ء�G�ڵؿ��к����ӵڶ�λ����G�ǹ�Ԫ�ء�HԪ����ɫ��Ӧ����ɫ����H��KԪ�ء�
��1��B��ԭ�ӽṹʾ��ͼΪ �� ��
��2������ˮ���Ӽ����γ����������ˮ���ӵķе����H2S�ķе㡣
��3�������Ǻ��м��Լ��Ĺ��ۻ�������γɹ��̿ɱ�ʾΪ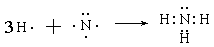 ?�� ?��
��4�����ʹ��ܺ�ǿ����Һ��Ӧ����Ӧ�Ļ�ѧ����ʽ��Si + H2O + 2KOH��K2SiO3 + 2H2����
��5��SO2���л�ԭ�ԣ��ܱ����Ը��������Һ��������Ӧ�����ӷ���ʽ��5SO2 + 2MnO4�� + 2H2O��2Mn2+ + 5SO42�� + 4H+?��
��6����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��a�з�Ӧ���ʵķ����෴�����������㷴Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ����Բ���˵�����÷�Ӧ�������С�Ŀ��淴Ӧ����ѹǿ���ٷ����仯ʱ����˵����b��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�c����˵����ƽ��ʱ�������ʵ�Ũ�Ȳ��ٷ����仯�������ֵ�Ũ��֮�䲻һ������ij�ֹ�ϵ��d����ȷ���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���������䣬�����ʵ����DZ仯�ģ�����e����˵������˴�ѡbe��
��7��ԭ����и���ʧȥ���ӣ�������ڸ���ͨ��缫��Ӧʽ��CH4��10OH���D8e����CO32����7H2O��
�����������Ǹ߿��еij������ͣ������ۺ���ǿ�������߿��������ڼ���ѧ����ѧϰ��Ȥ��ѧϰ�����ԡ���Ҳ����������ѧ�������������������ѧ����Ӧ��������ѧϰЧ�ʡ������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬�Ƚ�ȫ�濼��ѧ���й�Ԫ���ƶ�֪ʶ���������֪ʶ������������ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������
�����Ѷȣ�һ��
5��ѡ���� ij����Ԫ������������Ӧˮ����ķ���ʽ��H2RO3�������⻯��ķ���ʽ��
A��RH4
B��RH3
C��H2R
D��HR
�ο��𰸣�A
�������������Ԫ������������Ӧˮ����ķ���ʽ��H2RO3��������ǣ�4�ۣ�������ͼ��ǣ�4�ۣ����⻯����RH4����ѡA��
�����Ѷȣ�һ��
| 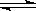 2AE2��g���Ѵﵽƽ��״̬����?������ţ�
2AE2��g���Ѵﵽƽ��״̬����?������ţ�