1ЎўМоҝХМв јЧЛбјЧхҘЛ®Ҫв·ҙУҰ·ҪіМКҪОӘЈәHCOOCH3 + H2O  ?HCOOH + CH3OH ЁC QЈЁQ>0Ј©
?HCOOH + CH3OH ЁC QЈЁQ>0Ј©
ДіРЎЧйНЁ№эКөСйСРҫҝёГ·ҙУҰЈЁ·ҙУҰ№эіМЦРМе»эұд»ҜәцВФІ»јЖЈ©ЎЈ·ҙУҰМеПөЦРёчЧй·ЦөДЖрКјБҝИзЧуПВұнЎЈјЧЛбјЧхҘЧӘ»ҜВКФЪОВ¶ИT1ПВЛж·ҙУҰКұјдЈЁtЈ©өДұд»ҜИзУТПВНјЈә
Чй·Ц
| ОпЦКөДБҝ/mol
|
HCOOCH3
| 1.00
|
H2O
| 1.99
|
HCOOH
| 0.01
|
CH3OH
| 0.52
|
ЙПКц·ҙУҰөДЖҪәвіЈКэұнҙпКҪОӘK=_______________________ЎЈ
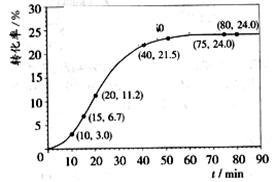
јЖЛг15~20min·¶О§ДЪЈәјЧЛбјЧхҘөДјхЙЩБҝОӘ?molЈ¬јЧЛбјЧхҘөДЖҪҫщ·ҙУҰЛЩВКОӘ ?mol/minЈ»80~90min·¶О§ДЪјЧЛбјЧхҘөДЖҪҫщ·ҙУҰЛЩВКОӘ___________ mol/minЎЈ
ТАҫЭТФЙПКэҫЭЈ¬НЖ¶ПёГ·ҙУҰФЪ10minәу·ҙУҰЛЩВКСёЛЩјУҝмөДФӯТтЈә??ЎЈ
ЖдЛыМхјюІ»ұдЈ¬МбёЯОВ¶ИОӘT2Ј¬ФЪҙрМвҝЁҝтНјЦР»ӯіцОВ¶ИT2ПВјЧЛбјЧхҘЧӘ»ҜВКЛж·ҙУҰКұјдұд»ҜөДФӨЖЪҪб№ыКҫТвНјЎЈ
ІОҝјҙр°ёЈә ЈЁ1·ЦЈ©0.045 Ј¬ 9.0ЎБ10-3Ј¬? 0ЈЁ3·ЦЈ©
ЈЁ1·ЦЈ©0.045 Ј¬ 9.0ЎБ10-3Ј¬? 0ЈЁ3·ЦЈ©
ёГ·ҙУҰЦРјЧЛбҫЯУРҙЯ»ҜЧчУГЈ¬јЧЛбБҝЦрҪҘФц¶аЈ¬ҙЯ»ҜР§№ыПФЦшЈ¬·ҙУҰЛЩВКГчПФФцҙуЎЈЈЁ2·ЦЈ©
 ЈЁ2·ЦЈ©
ЈЁ2·ЦЈ©
ұҫМвҪвОцЈәЈЁ1Ј©»ҜС§ЖҪәвіЈКэКЗФЪТ»¶ЁМхјюПВЈ¬өұҝЙДж·ҙУҰҙпөҪЖҪәвЧҙМ¬КұЈ¬ЙъіЙОпЕЁ¶ИөДГЭЦ®»эәН·ҙУҰОпЕЁ¶ИөДГЭЦ®»эөДұИЦөЈ¬ЛщТФёщҫЭ·ҙУҰөД»ҜС§·ҪіМКҪҝЙЦӘЈ¬ЖҪәвіЈКэ ЎЈ
ЎЈ
ЈЁ2Ј©ёщҫЭНјЦРөДЧӘ»ҜВКҝЙЦӘЈ¬15minКұјЧЛбјЧхҘөДЧӘ»ҜВККЗ6.7%Ј¬ФтПыәДјЧЛбјЧхҘөДОпЦКөДБҝКЗ0.067molЎЈ20minКұјЧЛбјЧхҘөДЧӘ»ҜВККЗ11.2%Ј¬ФтПыәДјЧЛбјЧхҘөДОпЦКөДБҝКЗ0.112molЈ¬ЛщТФФЪ15Ў«20minДЪјЧЛбјЧхҘјхЙЩБЛ0.112molЈӯ0.067molЈҪ0.045ЎЈФтјЧЛбјЧхҘөДЖҪҫщ·ҙУҰЛЩВКОӘ0.045molЎВ5minЈҪ0.009mol/minЈ»ёщҫЭНјПсҝЙЦӘЈ¬80minәу·ҙУҰОпөДЧӘ»ҜВКІ»ФЩ·ўЙъұд»ҜЈ¬ЛөГч·ҙУҰТСҫӯҙпөҪЖҪәвЧҙМ¬Ј¬Фт80Ў«90min·¶О§ДЪјЧЛбјЧхҘөДЖҪҫщ·ҙУҰЛЩВКОӘ0ЎЈ
ЈЁ3Ј©УЙУЪФЪёГ·ҙУҰЦРјЧЛбҫЯУРҙЯ»ҜЧчУГЈ¬ЛжЧЕ·ҙУҰөДҪшРРЈ¬јЧЛбБҝЦрҪҘФц¶аЈ¬ҙЯ»ҜР§№ыПФЦшЈ¬·ҙУҰЛЩВКГчПФФцҙуЎЈ
ЈЁ4Ј©Хэ·ҙУҰКЗОьИИ·ҙУҰЈ¬ЛщТФЙэёЯОВ¶ИЈ¬·ҙУҰОпөДЧӘ»ҜВКФцҙуЎЈЗТ·ҙУҰЛЩВКҝмЈ¬ҙпөҪЖҪәвөДКұјдЙЩЈ¬јҙНјПсКЗЈЁјыҙр°ёЈ©ЎЈ
өгЖАЈәёГМвКЗёЯҝјЦРөДіЈјыМвРНЈ¬КфУЪЦРөИДС¶ИөДКФМвЎЈКФМвМщҪьёЯҝјЈ¬ЧЫәПРФЗҝЈ¬ФЪЧўЦШ¶ФС§Йъ»щҙЎЦӘК¶№®№МУлСөБ·өДН¬КұЈ¬ІаЦШ¶ФС§ЙъДЬБҰөДЕаСшУлҪвМв·Ҫ·ЁөДЦёөјәНСөБ·Ј¬ЦјФЪҝјІйС§ЙъБй»оФЛУГ»щҙЎЦӘК¶ҪвҫцКөјКОКМвөДДЬБҰЈ¬УРАыУЪЕаСшС§ЙъөДВЯјӯНЖАнДЬБҰәНУҰКФДЬБҰЎЈ
ұҫМвДС¶ИЈәА§ДС
2ЎўСЎФсМв Т»¶ЁОВ¶ИПВЈ¬ФЪ2 LГЬұХИЭЖчЦР·ўЙъПВБР·ҙУҰЈә4NO2(g)Ј«O2(g) 2N2O5(g)Ј»ТСЦӘёГ·ҙУҰөДЖҪәвіЈКэЈәK300 ЎжЈҫK350 ЎжЈ¬ЗТn(NO2)(өҘО»Јәmol)ЛжКұјдұд»ҜИзПВұнЈә
2N2O5(g)Ј»ТСЦӘёГ·ҙУҰөДЖҪәвіЈКэЈәK300 ЎжЈҫK350 ЎжЈ¬ЗТn(NO2)(өҘО»Јәmol)ЛжКұјдұд»ҜИзПВұнЈә
Кұјд(s)
| 0
| 500
| 1000
| 1500
|
t1Ўж
| 20
| 13.96
| 10.08
| 10.08
|
t2Ўж
| 20
| a
| b
| c
|
?
ПВБРЛө·ЁТ»¶ЁХэИ·өДКЗЈЁ?Ј©
AЈ®Хэ·ҙУҰОӘОьИИ·ҙУҰ
BЈ®Из№ыt2ЎжЈјt1ЎжЈ¬ДЗГҙaЈҫbЈҪcЈ¬ЗТaЈҪ10Ј«0.5b
CЈ®Из№ыt2ЎжЈјt1ЎжЈ¬ДЗГҙt2ЎжҙпөҪЖҪәвөДКұјдҪйУЪ1 000 sЦБ1 500 sЦ®јд
DЈ®Из№ыt2ЎжЈҫt1ЎжЈ¬ДЗГҙbЈҫ10.08
ІОҝјҙр°ёЈәD
ұҫМвҪвОцЈәAПоЈ¬ОВ¶ИФҪөНЈ¬ЖҪәвіЈКэФҪҙуЈ¬ЛөГчХэ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬ҙнОуЈ»BПоЈ¬ҪөОВЈ¬·ҙУҰЛЩВКјхВэЈ¬1 000 sКұОҙЖҪәвЈ¬bУлcІ»ПаөИЈ¬ҙнОуЈ»CПоЈ¬t2ЎжКұЈ¬УЙУЪ·ҙУҰЛЩВКјхРЎЈ¬ҙпөҪЖҪәвЛщУГКұјдіӨЈ¬ҙуУЪ1 000 sЈ¬ө«ОЮ·ЁИ·¶ЁҙпөҪЖҪәвЛщРиКұјдЈ»DПоЈ¬ЙэОВЈ¬ЖҪәвЧуТЖЈ¬ЦВК№bЈҫ10.08Ј¬ХэИ·ЎЈ
ұҫМвДС¶ИЈәТ»°г
3ЎўСЎФсМв ФЪТ»¶ЁОВ¶ИПВҝЙДж·ҙУҰH2ЈЁgЈ©+I2ЈЁgЈ©?2HIЈЁgЈ©ҙпөҪЖҪәвөДұкЦҫКЗЈЁЎЎЎЎЈ©
AЈ®УР1molH-Hјь¶ПБСЈ¬Н¬КұУР1molI-IјьРОіЙ
BЈ®ИЭЖчДЪС№ЗҝІ»ФЩЛжКұјд¶шұд»Ҝ
CЈ®өҘО»КұјдДЪ·ҙУҰөфnmolI2Н¬КұЙъіЙ2nmolHI
DЈ®H2ЎўI2ЎўHIөДЕЁ¶ИЦ®ұИОӘ1Јә1Јә2
ІОҝјҙр°ёЈәAЎўУР1mol H-Hјь¶ПБСөДН¬КұУЦУР1 mol I-IјьРОіЙЈ¬ЛөГчХэДж·ҙУҰЛЩВКПаөИЈ¬ҙпөҪБЛЖҪәвЧҙМ¬Ј¬№КAХэИ·Ј»
BЎў·ҙУҰБҪұЯЖшМеөДМе»эІ»ұдЈ¬С№ЗҝІ»КЗұдБҝЈ¬ЛщТФС№ЗҝІ»ұдЈ¬ОЮ·ЁЕР¶ПКЗ·сҙпөҪЖҪҫІЧҙМ¬Ј¬№КBҙнОуЈ»
CЎўұнКҫөД¶јКЗХэ·ҙУҰЛЩВКЈ¬ОЮ·ЁЕР¶ПХэДж·ҙУҰЛЩВККЗ·сПаөИЈ¬№КCҙнОуЈ»
DЎўёчЧй·ЦЕЁ¶ИЦ®ұИЈ¬ОЮ·ЁЕР¶ПЕЁ¶ИКЗ·с»№»бІ»ұдЈ¬ОЮ·ЁЕР¶ПКЗ·сҙпөҪЖҪәвЧҙМ¬Ј¬№КDҙнОуЈ»
№КСЎЈәAЈ®
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәТ»°г
4ЎўМоҝХМв МјЛб¶юјЧхҘ(DMC)КЗТ»ЦЦҪьДкАҙКЬөҪ№г·ә№ШЧўөД»·ұЈРНВМЙ«»Ҝ№ӨІъЖ·ЎЈФЪҙЯ»ҜјБЧчУГПВЈ¬ҝЙУЙјЧҙјәНCO2ЦұҪУәПіЙDMCЈәCO2 + 2CH3OH Ўъ CO(OCH3)2 + H2OЈ¬ө«јЧҙјЧӘ»ҜВКНЁіЈІ»»бі¬№э1%КЗЦЖФјёГ·ҙУҰЧЯПт№ӨТө»ҜөДЦчТӘФӯТтЎЈДіСРҫҝРЎЧйФЪЖдЛыМхјюІ»ұдөДЗйҝцПВЈ¬НЁ№эСРҫҝОВ¶ИЎў·ҙУҰКұјдЎўҙЯ»ҜјБУГБҝ·Цұр¶ФЧӘ»ҜКэ(TON)өДУ°ПмАҙЖАјЫҙЯ»ҜјБөДҙЯ»ҜР§№ыЎЈјЖЛ㹫КҪОӘЈәTON=ЧӘ»ҜөДјЧҙјөДОпЦКөДБҝ/ҙЯ»ҜјБөДОпЦКөДБҝЎЈ
ЈЁ1Ј©ТСЦӘ25ЎжКұЈ¬јЧҙјәНDMCөДұкЧјИјЙХИИ·ЦұрОӘЎчH1әНЎчH2Ј¬ФтЙПКц·ҙУҰФЪ25ЎжКұөДмКұдЎчH3=_____ЎЈ
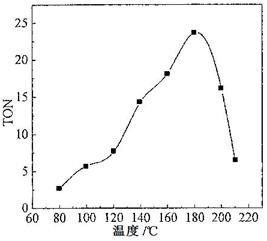
ЈЁ2Ј©ёщҫЭ·ҙУҰОВ¶И¶ФTONөДУ°ПмНјЈЁПВЧуНјЈ©ЕР¶ПёГ·ҙУҰөДмКұдЎчH________0ЈЁМоЎ°>ЎұЎўЎ°=Ўұ»тЎ°<ЎұЈ©Ј¬АнУЙКЗ________________________________ЎЈ
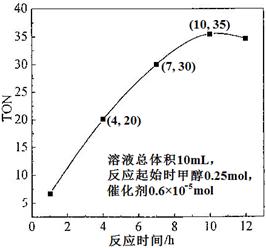
ЈЁ3Ј©ёщҫЭ·ҙУҰКұјд¶ФTONөДУ°ПмНјЈЁЙПУТНјЈ©Ј¬ТСЦӘИЬТәЧЬМе»э10mLЈ¬·ҙУҰЖрКјКұјЧҙј0.25molЈ¬ҙЯ»ҜјБ0.6ЎБ10ЎӘ5 molЈ¬јЖЛгёГОВ¶ИПВЈ¬4Ў«7 hДЪDMCөДЖҪҫщ·ҙУҰЛЩВКЈә________Ј»јЖЛг10 hКұЈ¬јЧҙјөДЧӘ»ҜВКЈә________ЎЈ
ЈЁ4Ј©ёщҫЭёГСРҫҝРЎЧйөДКөСйј°ҙЯ»ҜјБУГБҝ¶ФTONөДУ°ПмНјЈЁПВНјЈ©Ј¬ЕР¶ППВБРЛө·ЁХэИ·өДКЗ___?__ЎЈ

a. УЙјЧҙјәНCO2ЦұҪУәПіЙDMCЈ¬ҝЙТФАыУГјЫБ®ТЧөГөДјЧҙј°СУ°Пм»·ҫіөДОВКТЖшМеCO2ЧӘ»ҜОӘЧКФҙЈ¬ФЪЧКФҙСӯ»·АыУГәН»·ҫіұЈ»Ө·ҪГж¶јҫЯУРЦШТӘТвТе
b. ФЪ·ҙУҰМеПөЦРМнјУәПККөДНСЛ®јБЈ¬Ҫ«МбёЯёГ·ҙУҰөДTON
c. өұҙЯ»ҜјБУГБҝөНУЪ1.2ЎБ10ЎӘ5 molКұЈ¬ЛжЧЕҙЯ»ҜјБУГБҝөДФцјУЈ¬јЧҙјөДЖҪәвЧӘ»ҜВКПФЦшМбёЯ
d. өұҙЯ»ҜјБУГБҝёЯУЪ1.2ЎБ10ЎӘ5 molКұЈ¬ЛжЧЕҙЯ»ҜјБУГБҝөДФцјУЈ¬DMCөДІъВК·ҙ¶шјұҫзПВҪө
ІОҝјҙр°ёЈәЈЁ15·ЦЈ©
ЈЁ1Ј©2ЎчH1 ЎӘ ЎчH2?ЈЁ3·ЦЈ©
ЈЁ2Ј©< ЈЁ2·ЦЈ©?ҫӯ№эПаН¬өД·ҙУҰКұјдЈ¬ОВ¶ИҪПөНКұЈ¬·ҙУҰОҙҙпөҪЖҪәвЈ»ОВ¶ИҪПёЯКұЈ¬·ҙУҰТСҙпөҪЖҪәвЈ¬ЛжЧЕОВ¶ИЙэёЯЈ¬TONјхРЎЈ¬јҙЖҪәвПтЧуТЖ¶ҜЈ¬ЛөГчёГ·ҙУҰ·ЕИИЈЁ3·ЦЈ©
ЈЁ3Ј©1ЎБ10-3 molЎӨL-1ЎӨh-1ЈЁ 2·ЦЈ© 8.4ЎБ10-2 % ЈЁ2·ЦЈ©
ЈЁ4Ј©abЈЁ3·ЦЈ©
ұҫМвҪвОцЈә
ЈЁ1Ј©ёщҫЭ·ҙУҰўЩCH3OH(l)+1.5O2(g)=CO2(g)+2H2O(l)? ҰӨH1Ј¬ўЪCO(OCH3)2(l)+3O2(g)=3CO2(g)+3H2O(l) ?ҰӨH1Ј¬ёщҫЭёЗЛ№¶ЁВЙУРДҝұк·ҙУҰөИУЪўЩЎБ2-ўЪЈ¬№КУРҰӨH3=2ҰӨH1-ҰӨH2
ЈЁ2Ј©ёщҫЭНјҝЙЦӘЈ¬ОВ¶ИЙэёЯЈ¬ЖҪәвДжПтТЖ¶ҜЈ¬№КХэ·ҙУҰ·ЕИИҰӨH<0Ј»
ЈЁ3Ј©4hЈ¬TON=20Ј¬7hЈ¬TON=30Ј¬ҰӨTON=10Ј¬ҰӨјЧҙј=10ЎБ0.6ЎБ10-5mol=0.6ЎБ10-4molЈ¬ЛЩВКОӘ0.6ЎБ10-4molЎВ0.01LЎВ3h=2ЎБ10-3 molЎӨL-1ЎӨh-1Ј¬10hЈ¬ЧӘ»ҜөДјЧҙјОӘ35ЎБ0.6ЎБ10-5mol=2.1ЎБ10-4molЈ¬ЧӘ»ҜВКОӘ2.1ЎБ10-4molЎВ0.25mol=8.4ЎБ10-2 %
ЈЁ4Ј©aЎўХэИ·Ј¬bЎўјхЙЩЛ®Ј¬К№ЖҪәвХэПтТЖ¶ҜЈ¬ХэИ·Ј»cdЎўTONәНЧӘ»ҜВКІ»КЗТ»СщЈ¬ҙнОуЈ»
ұҫМвДС¶ИЈәТ»°г
5ЎўМоҝХМв ТСЦӘ2SO2ЈЁgЈ©Ј«O2ЈЁgЈ© 2SO3ЈЁgЈ©Ј»ЎчHЈј0өДКөСйКэҫЭИзПВұнЈә
2SO3ЈЁgЈ©Ј»ЎчHЈј0өДКөСйКэҫЭИзПВұнЈә
ОВ¶И
| І»Н¬С№ЗҝПВSO2өДЧӘ»ҜВКЈЁ%Ј©
|
1ЎБ105Pa
| 5ЎБ105Pa
| 1ЎБ106Pa
| 5ЎБ106Pa
| 1ЎБ107Pa
|
450Ўж
| 97.5
| 98.9
| 99.2
| 99.6
| 99.7
|
550Ўж
| 85.6
| 92.9
| 94.9
| 97.7
| 98.3
|
ЈЁ1Ј©УҰСЎөДОВ¶ИКЗ?ЎЈ
ЈЁ2Ј©УҰІЙУГөДС№ЗҝКЗ?Ј¬АнУЙКЗ?ЎЈ
ЈЁ3Ј©ФЪәПіЙөДSO3№эіМЦРЈ¬І»РиТӘ·ЦАліцSO3өДФӯТтКЗ?ЎЈ
ІОҝјҙр°ёЈәЈЁ1Ј©450ЎжЈ»ЈЁ2Ј©1ЎБ105Pa?ТтОӘіЈС№ПВSO2өДЧӘ»ҜВКТСҫӯәЬёЯЈ¬ИфІЙУГҪПҙуөДС№ЗҝЈ¬SO2өДЧӘ»ҜВКМбёЯәЬЙЩЈ¬ө«РиТӘ¶ҜБҰёьҙ󣬶ФЙиұёөДТӘЗуёьёЯЈ»ЈЁ3Ј©ТтОӘSO2өДЧӘ»ҜВКұИҪПёЯЈ¬ҙпөҪЖҪәвәуөД»мәПЖшМеЦРSO2өДУаБҝәЬЙЩЈ¬№КІ»РиТӘ·ЦАлSO3ЎЈ
ұҫМвҪвОцЈә№ӨТөЙъІъЦРјИТӘҝјВЗ·ҙУҰЛЩВКҝмЈ¬УЦТӘҝјВЗФӯБПЧӘ»ҜВКёЯЈ¬Н¬КұТІТӘҝјВЗКөПЦМхјюөДПЮЦЖЎЈөұЛьГЗіцПЦГ¬¶ЬКұЈ¬БҪХЯ¶јТӘјж№ЛЈ¬МШұрТӘККУҰҙЯ»ҜјБөД»оРФЎЈёГ·ҙУҰУләПіЙ°ұПаЛЖЈ¬ө«КөјКЗйҝцУЦІ»НкИ«ПаН¬Ј¬№КҪвМвКұУҰАнВЫБӘПөКөјКЈ¬ТАҫЭәПіЙSO3өДКөСйКэҫЭАҙҪвҙрЎЈёГ·ҙУҰУләПіЙ°ұөД·ҙУҰПаЛЖЈә¶јКЗЖшМеМе»эЛхРЎөД·ЕИИ·ҙУҰЈ¬ОВ¶ИЙэёЯУРАыУЪјУҝм·ҙУҰЛЩВКЈ¬ө«ҪөөНБЛ·ҙУҰОпөДЧӘ»ҜВКЈ¬ККТЛөДМхјюөДСЎФсРиТӘЧЫәПҝјВЗЎЈФцҙуС№ЗҝУРАыУЪјУҝм·ҙУҰЛЩВКЈ¬Н¬КұТІМбёЯБЛ·ҙУҰОпөДЧӘ»ҜВКЈ¬ө«С№Зҝ¶ФSO2өДЧӘ»ҜВКУ°ПмІ»ҙуЈ¬Н¬КұјУС№РиТӘ¶ҜБҰТтЛШЎўЙиұёДНС№ТтЛШЈ¬ЧЫәПҫӯјГР§ТжЈ¬ЙъІъ№эіМЦРІЙУГФЪіЈС№ПВҪшРРЧоәПАнЎЈУЙУЪSO2өДЧӘ»ҜВКұИҪПёЯЈ¬ҙпөҪЖҪәвәуөД»мәПЖшМеЦРSO2өДУаБҝәЬЙЩЈ¬№КІ»РиТӘ·ЦАлSO3ЎЈ
ұҫМвДС¶ИЈәТ»°г