1、实验题 二氧化铈 是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含
是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含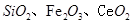 以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
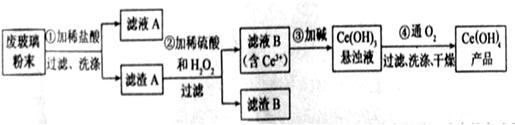
(1)洗涤滤渣A的目的是为了去除?(填离子符号),检验该离子是否洗净的方法是?。
(2)第②步反应的离子方程式是?,滤渣B的主要成分是?。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP?(填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器有?、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的
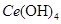 产品0.536g,加硫酸溶解后,用0.1000mol?
产品0.536g,加硫酸溶解后,用0.1000mol?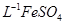 溶液(铈被还原为
溶液(铈被还原为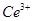 ),消耗25.00mL溶液,该产品中
),消耗25.00mL溶液,该产品中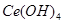 的质量分数为?。
的质量分数为?。
参考答案:(1) Fe3+?;取少量最后一次洗涤液于试管中,滴加2-3滴KSCN,如果不出现红色,则洗涤干净。(2)2CeO2+H2O2+6H+ =" 2" Ce3+ +O2↑+ 4H2O?;SiO2(3)不能;分液漏斗(4)97.01%
本题解析:(1)洗涤滤渣A的目的是为了去除 Fe3+ ,检验该离子是否洗净的方法是取少量最后一次洗涤液于试管中,滴加2-3滴KSCN,如果不出现红色,则洗涤干净;(2)第②步反应为二氧化铈氧化过氧化氢的反应,所以其离子反应方程式为:2CeO2+H2O2+6H+ =" 2" Ce3+ +O2↑+ 4H2O,由于二氧化硅不与酸反应,所以滤渣B的主要成分是二氧化硅,(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,根据萃取的条件可以知道,TBP不与水互溶;实验室进行萃取操作是用到的主要玻璃仪器有分液漏斗、烧杯、玻璃棒、量筒等;(4)用0.1000mol?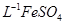 溶液(铈被还原为
溶液(铈被还原为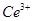 ),消耗25.00mL溶液,所以铈质量为=0.1000×0.025×140g=0.35g,所以
),消耗25.00mL溶液,所以铈质量为=0.1000×0.025×140g=0.35g,所以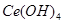 的质量为0.35g×208/140=0.52g,故
的质量为0.35g×208/140=0.52g,故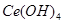 的质量分数=0.52/0.536×100%=97.01%。
的质量分数=0.52/0.536×100%=97.01%。
点评:本题考查了元素及其化合物,该考点是高考考查的重点,本题由一定的综合性,该题有利于培养学生的分析能力,该题难度不大。
本题难度:困难
2、选择题 合金比纯金属制成的金属材料的优点是
[? ]
①合金的硬度一般比它的各成分金属的大
②一般地,合金的熔点比它的各成分金属的更低
③合金比纯金属的导电性更强
④合金比纯金属的应用范围更广泛
A.①②③④
B.②③④
C.①②④
D.①②
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列物质属于复合材料的是
A.普通玻璃
B.普通钢
C.玻璃钢
D.镁铝合金
参考答案:C
本题解析:含有两种以上类型的材料称为复合材料。A、普通玻璃属硅酸盐产品,属无机非金属材料,错误;B、普通钢是铁、碳合金,不是复合材料,错误;C、玻璃钢是由玻璃与树脂混合成的,前者是无机非金属材料,后者是有机高分子合成材料,故玻璃钢是两种材料复合成的,正确;D、镁铝合金属于金属材料,不是复合材料,错误,答案选C。
本题难度:一般
4、填空题 (1)为了提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO4・7H2O进行消毒、净化,以改善水质,其原因是_____________________________。
(2)为了延长液氯杀菌时间,某些自来水厂在用液氯进行消毒处理时,还加入少量液氨,其反应的化学方程式为:NH3+HClO H2O+NH2Cl(一氯氨)。已知NH2Cl比HClO稳定,试分析加液氨能延长液氯杀菌时间的原因是______________________________。
H2O+NH2Cl(一氯氨)。已知NH2Cl比HClO稳定,试分析加液氨能延长液氯杀菌时间的原因是______________________________。
参考答案:(1)氯气杀菌、亚铁盐水解产生的胶体吸附悬浮杂质?
(2)加氨后,次氯酸的释放经可逆反应:NH3+HClO H2O+NH2Cl后相当于缓释作用
H2O+NH2Cl后相当于缓释作用
本题解析:(1)Cl2与FeSO4・7H2O同时使用可以改善水质的原因为:Cl2+H2O HCl +HClO,HClO具有强氧化性,能杀死水中的细菌,起消毒的作用。
HCl +HClO,HClO具有强氧化性,能杀死水中的细菌,起消毒的作用。
Cl2还可将Fe2+氧化成Fe3+:Cl2+2Fe2+====2Cl-+2Fe3+。Fe3+水解:Fe3++3H2O Fe(OH)3+3H+,生成Fe(OH)3胶体。Fe(OH)3胶体具有较强的吸附性能,可吸附水中的悬浮杂质,并能形成沉淀,使水净化。
Fe(OH)3+3H+,生成Fe(OH)3胶体。Fe(OH)3胶体具有较强的吸附性能,可吸附水中的悬浮杂质,并能形成沉淀,使水净化。
(2)根据(1)中的分析,起杀菌消毒作用的是HClO,由题意可知NH2Cl的稳定性大于HClO,向含有Cl2的自来水加入NH3之后会发生如下反应:HClO+NH3 H2O+NH2Cl,从而使不稳定的HClO部分转化为较稳定的NH2Cl。在消毒过程中,随着HClO浓度的降低,上述平衡将向左移动,HClO得以补充,从而延长了液氯的杀菌时间。
H2O+NH2Cl,从而使不稳定的HClO部分转化为较稳定的NH2Cl。在消毒过程中,随着HClO浓度的降低,上述平衡将向左移动,HClO得以补充,从而延长了液氯的杀菌时间。
本题难度:简单
5、选择题 下列说法正确的是
[? ]
A.合金钢不含非金属元素
B.合金钢和碳素钢都含碳元素
C.碳素钢是由铁和碳元素组成的化合物
D.碳素钢是由铁和碳通过化合反应形成的
参考答案:B
本题解析:
本题难度:简单