1、选择题 某主族元素R的原子其电子式可用下式表示: 。该元素组成的以下物质,其分子式肯定错误的是
。该元素组成的以下物质,其分子式肯定错误的是
[? ]
A.最高价氧化物分子式为R2O5
B.含氧酸分子式为 HRO3
C.含氧酸分子式为H3RO4
D.气态氢化物分子式为RH5
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列化学用语表达错误的是( )
A.S2-的结构示意图: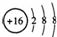
B.NH3的结构式: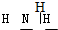
C.CO2分子的比例模型:
D.CaCl2的电子式: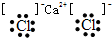
参考答案:A.硫离子核内含有16个质子,核外有3个电子层,最外层有8个电子,其结构示意图: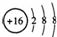 ,故A正确;
,故A正确;
B.结构式中只标出共价键不标出孤电子对,所以氨气的结构式为: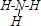 ,故B正确;
,故B正确;
C.二氧化碳是直线型分子,故C错误;
D.氯化钙是离子化合物,其电子式为: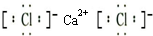 ,故D正确;
,故D正确;
故选C.
本题解析:
本题难度:一般
3、填空题 研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是__________。 C60和金刚石都是碳的同素异形体,二者比较熔点高的是___________,原因是__________________________。
(2)A、B均为短周期金属元素,依据下表数据,写出B的基态原子的电子排布式__________________。
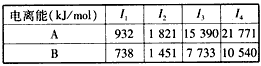
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1-d9排布时,有颜色。如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+_________(填“无”或 “有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 每个COCl2分子内含有______个σ键,________个π键。其中心原子采取_________ 杂化轨道方式。
每个COCl2分子内含有______个σ键,________个π键。其中心原子采取_________ 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s) = Fe(s) +5CO(g),反应过程中,断裂的化学键只有 配位键,则形成的化学键类型是_______________。
参考答案:(1)N>C>Si;金刚石;金刚石为原子晶体,而C60为分子晶体
(2)1s22s22p63s2
(3)有
(4)①3;1;sp2②金属键
本题解析:
本题难度:一般
4、选择题  科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关推测肯定不正确的是(?)
科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关推测肯定不正确的是(?)
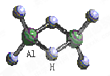

A.Al2H6跟水的反应可能是氧化还原反应,产物之一可能是氢氧化铝

B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.Al2H6分子是极性分子
D.氢铝化合物可能成为未来的储氢材料和火箭燃料
参考答案:C
本题解析:略
本题难度:一般
5、选择题 下列有关说法不正确的是
[?]
A.由乙烯分子组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n
B.乙烯的电子式为 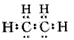
C.从乙烯与溴发生加成反应生成1,2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高
参考答案:B
本题解析:
本题难度:一般