1、选择题 在相同温度下,100mL?0.01mol/L醋酸与10mL?0.1mol/L醋酸相比,下列数值前者大于后者的是( )
A.中和时所需NaOH的量
B.电离程度
C.H+浓度
D.醋酸的物质的量
参考答案:B
本题解析:
本题难度:一般
2、简答题 下列化合物:①HCl?②NaOH?③CH3COOH?④NH3?H2O?⑤CH3COONa?⑥NH4Cl
(1)属于弱电解质的是______,溶液呈碱性的有______(填序号).
(2)常温下0.01mol/L?HCl溶液的PH=______;pH=11的CH3COONa溶液中由水电离产生的c(OH-)=______.
(3)用离子方程式表示CH3COONa溶液呈碱性的原因______,其溶液中离子浓度按由大到小的顺序为______.
(4)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的PH仍相等,则m______n?(填“大于、等于、小于”).
(5)常温下,向100mL?0.01mol?L-1HA溶液逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
①由图中信息可知HA为______酸(填“强”或“弱”).
②K点对应的溶液中,c(M+)+c(MOH)=______mol?L-1.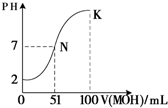
参考答案:(1)在水溶液里和熔融状态下只有部分电离的电解质是弱电解质,属于弱电解质的是一水合氨和醋酸,碱或强碱弱酸盐其溶液都呈碱性,氢氧化钠和氨水、醋酸钠溶液都呈碱性,故选:③④、②④⑤;
(2)pH=-lgc(H+)=-lg0.01=2,醋酸钠促进水电离,醋酸钠溶液中氢离子浓度为10-11mol/L,根据水的离子积常数知,氢氧根离子浓度等于10-3?mol/L,
故答案为:2、10-3?mol/L;
(3)醋酸钠是强碱弱酸盐,醋酸根离子水解生成醋酸,导致溶液中氢氧根离子浓度大于氢离子浓度而使其溶液呈碱性,水解离子方程式为:CH3COO?+H2O?CH3COOH+OH?,溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒,c(Na+)+c(H+)=c(CH3COO?)+c(OH-),则c(Na+)>c(CH3COO?),所以离子浓度大小顺序是c(Na+)>c(CH3COO?)>c(OH-)>c(H+),
故答案为:CH3COO?+H2O?CH3COOH+OH?,c(Na+)>c(CH3COO?)>c(OH-)>c(H+);
(4)醋酸是弱电解质,氯化氢是强电解质,醋酸存在电离平衡,氯化氢不存在电离平衡,将等pH的醋酸和盐酸稀释后溶液的pH仍然相等,则盐酸稀释的倍数小于醋酸,故答案为:小于;
(5)①根据图象知,0.01mol?L-1HA溶液中PH=2,氢离子浓度等于酸浓度,所以该酸是强酸,故答案为:强;
?②K点时,加入的MOH的物质的量=0.02mol?L-1×0.1L=0.002mol,混合溶液的体积是0.2L,根据物料守恒知,c(M+)+c(MOH)=0.002mol0.2L=0.01mol/L,故答案为:0.01.
本题解析:
本题难度:一般
3、选择题 下列实验能达到预期目的的是?(?)
编号
| 实验内容
| 实验目的
|
A
| 室温下,用pH试纸分别测定浓度为0.1mol・L-1NaClO溶液和0.1mol・L-1CH3COONa溶液的pH
| 比较HClO和CH3COOH的酸性强弱
|
B
| 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅
| 证明Na2CO3溶液中存在水解平衡
|
C
| 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀
| 证明在相同温度下的Ksp:
Mg(OH)2 >Fe(OH)3
|
D
| 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大
| 证明非金属性S>C
参考答案:B
本题解析:A.NaOH是强碱,HClO、CH3COOH是弱酸,因此它们产生的盐都是强碱弱酸盐,水解使溶液显碱性。但是NaClO溶液水解产生的HClO有漂白性,因此不能通过用PH试纸测定溶液的pH比较HClO和CH3COOH的酸性强弱。错误。B. Na2CO3是强碱弱酸盐,水解消耗水电离产生的H+而使溶液显碱性,因此向该盐的水溶液中滴加酚酞变为红色。若向含有酚酞的Na2CO3溶液中加入少量BaC12固体,会发生反应:CO32-+Ba2+=BaCO3↓,使CO32-的水解平衡逆向移动。水解程度减小,所以溶液的减小减弱,溶液红色变浅。正确。C. 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀。但是该沉淀存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),当再滴加2滴0.1 mol/LFeCl3溶液时由于,c(Fe3+)・c(OH-)≥Ksp [Fe(OH)3],所以又生成红褐色沉淀。由于Mg(OH)2 和Fe(OH)3的构型不同,因此这只能证明沉淀在溶液中存在沉淀溶解平衡,而不能证明其Ksp的大小。错误。D.证明元素的非金属性的强弱,要看其最高价氧化物对应的水化物的酸性强弱。Na2SO3不是S的最高价含氧酸的钠盐。错误。 Mg2+(aq)+2OH-(aq),当再滴加2滴0.1 mol/LFeCl3溶液时由于,c(Fe3+)・c(OH-)≥Ksp [Fe(OH)3],所以又生成红褐色沉淀。由于Mg(OH)2 和Fe(OH)3的构型不同,因此这只能证明沉淀在溶液中存在沉淀溶解平衡,而不能证明其Ksp的大小。错误。D.证明元素的非金属性的强弱,要看其最高价氧化物对应的水化物的酸性强弱。Na2SO3不是S的最高价含氧酸的钠盐。错误。
本题难度:一般
4、简答题 在常温下,0.1mol/L一元酸HB溶液的PH=3.试回答下列问题:
(1)HB在水溶液中的电离方程式为______,100mL0.1mol/L一元酸HB溶液和0.1mol/LNaOH溶液恰好完全反应时,所需NaOH溶液的体积为______mL.
(2)在常温下,0.1mol/L一元酸HB溶液中由水电离出的H+物质的量浓度是______;若将温度改变到t℃(此时Kw=10-12),则t______25(<、>或=),该温度下0.1mol/L一元酸HB溶液中由水电离出的H+物质的量浓度______.
A.10-11mol/L?B.10-9mol/L?C.10-6mol/L?D.以上答案都不正确
(3)在常温下,将0.1mol/L一元酸HB溶液稀释100倍后,溶液的PH______5(<、>或=).
参考答案:(1)常温下,0.1mol/L一元酸HB溶液的PH=3,氢离子浓度小于酸浓度,所以该酸是弱酸,存在电离平衡,其电离方程式为:HB?H++B-,一元酸碱发生中和反应时,酸碱的物质的量相等,等浓度的酸碱混合恰好反应时,酸碱的体积应该相等,所以氢氧化钠的体积是100mL,
故答案为:HB?H++B-,100mL;
(2)酸溶液中水电离出的氢离子浓度等于酸溶液中氢氧根离子浓度,常温下,0.1mol/L一元酸HB溶液中氢离子浓度是0.001mol/L,根据水的离子积常数知,氢氧根离子浓度为10-11mol/L,则由水电离出的H+物质的量浓度
10-11mol/L,水的电离是吸热反应,升高温度促进水电离,水的离子积常数变大,当Kw=10-12>10-14,则此时温度大于常温,弱电解质的电离是吸热反应,升高温度促进弱酸电离,所以该温度下,弱酸的电离程度增大,该酸溶液中氢离子浓度未知,所以无法计算水电离出的氢离子浓度,
故答案为:10-11mol/L,>,D;
(3)弱酸溶液中存在电离平衡,加水稀释促进其电离,所以常温下,将0.1mol/L一元酸HB溶液稀释100倍后,溶液中氢离子浓度大于原来的十分之一,则溶液的PH<5,故答案为:<.
本题解析:
本题难度:一般
5、填空题 草酸(H2C2O4)是二元弱酸,25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。
(1)KHC2O4溶液呈__________性(填“酸”、“中”或“碱”)。
(2)下列化学方程式可能正确的是?。
A.
B.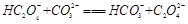
C.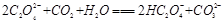
D.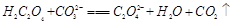
|
(3)常温下,向10 mL 0.01 mol・L-1H2C2O4溶液中滴加0.01 mol・L-1的KOH溶液V mL,回答下列问题:
①当V<10时,反应的离子方程式为______________________________________________。
②若溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
③当溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
④当V=20时,溶液中HC2O4-、C2O42-、H2C2O4、OH-的物质的量浓度从大到小的顺序为____________________________________________________________________________________。
参考答案:(1)酸?
(2)BD
(3)①H2C2O4+OH-=HC2O4-+H2O ?②=? > ?③KHC2O4? =
④c(C2O42-)>c(OH-)>c(HC2O4-)>c(H2C2O4)
本题解析:(1)KHC2O4溶液是强碱弱酸盐所以显碱性。
(2)由25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。数据可知酸性强弱H2C2O4> HC2O4-> H2CO3> HCO3-。所以BD正确。
(3)因为H2C2O4是弱酸,分步电离氢离子,与碱反应时,先生成HC2O4-,然后再生成C2O42-,所以当V<10时,反应的离子方程式为H2C2O4+OH-=HC2O4-+H2O。
②根据电荷守恒可知c(H+) +c(K+)=2c(C2O42-)+c(HC2O4-) +c(OH-)。若溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),则c(H+) =c(OH-)。 pH=7,V>10。
③当溶液中有c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),根据物料守恒可知溶液中只有一种溶质KHC2O4,此时V=10,若酸过量或者碱过量或者生成K2C2O4,则上式均不成立。
④当V=20时,,刚好反应生成K2C2O4,水解呈碱性。溶液中HC2O4-、C2O42-、H2C2O4、OH-的物质的量浓度从大到小的顺序为c(C2O42-)>c(OH-)>c(HC2O4-)>c(H2C2O4)。
本题难度:一般