1、选择题 若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是(? )
A? Mn+2HCl==MnCl2+H2↑?B? Mg+MnSO4==MgSO4+Mn
C? Mn+Cu(NO3)2==Mn(NO3)2+Cu? D? Fe+MnSO4==FeSO4+Mn
参考答案:D
本题解析:
本题难度:一般
2、填空题 铜是生物体必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式:________________________________________________________________________________________________________________________________________________。
(2)为了保护环境和节约资源,通常先用H2O2和稀硫酸的混合溶液溶出废旧印刷电路板中的铜,最终实现铜的回收利用。写出溶出铜的离子方程式:________________________________________________________________________________________________________________________________________________。
(3)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑,该反应的氧化剂是______________;当生成19.2 g Cu时,反应中转移的电子为__________mol。
6Cu+SO2↑,该反应的氧化剂是______________;当生成19.2 g Cu时,反应中转移的电子为__________mol。
(4)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜锈的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。试写出上述过程中负极的电极反应式:________________________________________________________________________________________________________________________________________________。
(5)研究性学习小组用“间接碘量法”测定某试样CuSO4・5H2O(不含能与I-反应的氧化性杂质)的含量。取a g试样配成100 mL溶液,每次取25.00 mL,滴加KI溶液后有白色碘化物沉淀生成。写出该反应的离子方程式:___________________________。继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫代硫酸钠标准溶液滴定,发生反应的化学方程式为I2+2Na2S2O3=2NaI+Na2S4O6,平均消耗c? mol/L的Na2S2O3溶液V mL。则试样中CuSO4・5H2O的质量分数为______________。
参考答案:(1)3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)Cu+H2O2+2H+=Cu2++2H2O
(3)Cu2O和Cu2S 0.3
(4)2Cu+4OH-+CO2-4e-=Cu2(OH)2CO3+H2O
(5)2Cu2++4I-=2CuI↓+I2 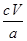 ×100%
×100%
本题解析:(2)H2O2在酸性条件下能将Cu氧化为Cu2+。(3)该反应中Cu2S和Cu2O中Cu的化合价均由+1价降低为Cu中的0价,Cu2S和Cu2O均为氧化剂,硫元素化合价由-2价升高到+4价,转移电子数为6个,故生成0.3 mol Cu时转移电子为0.3 mol。(4)Cu在负极失去电子形成Cu2+,Cu2+再与空气中的CO2、H2O 结合生成铜锈。(5)根据电子守恒得关系式:Cu2+~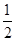 I2~Na2S2O3,故试样中CuSO4・5H2O的质量分数为
I2~Na2S2O3,故试样中CuSO4・5H2O的质量分数为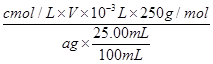 ×100%=
×100%=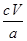 ×100%。
×100%。
本题难度:一般
3、选择题 Cu和稀硝酸反应中,若有63g 硝酸被还原了,则被氧化的铜的物质的量为
A.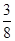 mol
mol
B.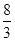 mol
mol
C.3mol
D.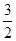 mol
mol
参考答案:D
本题解析:由m/M可知被还原的n(HNO3)=1mol,HNO3被还原为NO,Cu被氧化为Cu(NO)2,氮元素由+5价降为+2价,铜元素由0价升为+2价,设被氧化的n(Cu)=xmol,由电子得失守恒原理可知,1mol×[(+5)―(+2)]=xmol×[(+2)―0],解得:x=3/2,D项正确。
本题难度:一般
4、选择题 标准状况下,往100mL 0.2mol/L的FeBr2溶液中通入一定体积的Cl2,充分反应后,溶液中有50%的Br-被氧化。则通入的氯气的体积是(?)
A.0.224L
B.0.336L
C.0.448L
D.0.672L
参考答案:C
本题解析:
【错解分析】忽略离子还原性强弱。在氧化还原反应中,还原性(氧化性)越强的物质(或微粒)优先参与氧化还原反应。由于2Br- + Cl2=Br2 + 2Cl-,根据题意,有50%的Br-被氧化,即有0.02mol被氧化,因此通入的氯气的体积为0.224L。错选A。
【正解】由于Fe2+还原性比Br-强,当往FeBr2中通入氯气,发生的反应依次为:1)Cl2+2Fe2+=2Cl―+2Fe3+;2)Cl2+2Br―=2Cl―+Br2。因此溶液反应中反应的情况应该是:Fe2+被完全氧化并有50% Br― 被氧化。根据电子得失关系,Fe2+、Br―离子失去的电子总数(0.02mol+0.02mol=0.04mol)等于Cl2得到的电子总数。由于每个Cl2在反应中得到2个电子,因此Cl2的物质的量为0.02mol,其体积为0.448L。本题正确答案为C。(注:分析多种离子共存的溶液体系的电解问题时,也必须考虑离子反应次序――对于氧化性或还原性越强的离子,电解过程中一般优先放电。)
本题难度:一般
5、填空题 某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
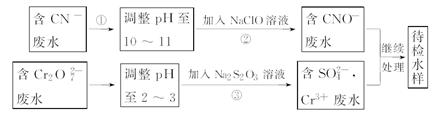
回答下列问题:
(1)上述处理废水流程中主要采用的方法是_____________。
(2)流程②中,反应后无气体放出,该反应的离子方程式为_______。
(3)含Cr3+废水需进一步处理,请你设计一个处理方案:_______。
(4)反应③中,每消耗0.4 mol Cr2O72-转移2.4 mol e-,该反应离子方程式为________。
参考答案:(1)氧化―还原法
(2)CN-+ClO-=CNO-+Cl- (3)调节废水pH,使其转化成Cr(OH)3沉淀除去(其他合理答案也可)
(4)3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O
本题解析:(2)由②中反应后无气体放出,可知其产物为Cl-和CNO-,根据电子守恒配平即可。(4)由消耗0.4 mol Cr2O72-转移2.4 mol e-,可知反应后铬转化为+3价,据此,再根据电子守恒写出离子方程式。
本题难度:一般