1��ѡ���� CuSO4��һ����Ҫ�Ļ���ԭ�ϣ����й��Ʊ�;����������ͼ��ʾ������˵������ȷ����
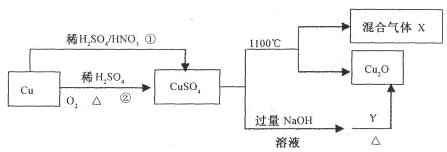
A�������;���٣�;���ڸ��õ���������ɫ��ѧ˼��
B��Y��������������Һ
C������;�����Ʊ�16g����ͭ������ԭ����������ʵ���Ϊ0.1 mol
D��;�������û�����H2SO4��HNO3���ʵ���֮�����Ϊ3:2
�ο��𰸣�C
���������A.������Ӧ��3Cu��8HNO3(ϡ)=2Cu(NO3)2��2NO����4H2O�������������Ⱦ��NO�����ڶ��ַ����ķ�ӦΪ2Cu+O2 2CuO. CuO+ H2SO4=CuSO4��H2O�����������Ⱦ���������ʡ����;���ڸ��õ���������ɫ��ѧ˼�롣��ȷ��B.��CuSO4��Һ�м��������NaOH��Һ�����Cu(OH)2����Һ��Ȼ���ټ��뺬��ȩ���������������ǡ���ȩ������Ȳ�������У��ͻᷢ��������ԭ��Ӧ�õ�ש��ɫ��Cu2O���������Y��������������Һ����ȷ��C. n(CuSO4)=16g��160g/mol=0.1mol.���������ڷ�Ӧʱ�Ĺ�ϵ��֪n(H2SO4)=0.1mol.�������ᷢ���IJ���������ԭ��Ӧ������D.;���ٷ�Ӧ�����ַ���ʽΪ3Cu��8H����2NO3��=3Cu2����2NO����4H2O������2mol��NO3������2mol�����ᣬ��ͬʱ�ṩ2mol��H+����8mol��H+��������������H+�����ʵ���Ϊ6mol�����С����������3mol����n(H2SO4):n(HNO3)=3:2.��ȷ��
2CuO. CuO+ H2SO4=CuSO4��H2O�����������Ⱦ���������ʡ����;���ڸ��õ���������ɫ��ѧ˼�롣��ȷ��B.��CuSO4��Һ�м��������NaOH��Һ�����Cu(OH)2����Һ��Ȼ���ټ��뺬��ȩ���������������ǡ���ȩ������Ȳ�������У��ͻᷢ��������ԭ��Ӧ�õ�ש��ɫ��Cu2O���������Y��������������Һ����ȷ��C. n(CuSO4)=16g��160g/mol=0.1mol.���������ڷ�Ӧʱ�Ĺ�ϵ��֪n(H2SO4)=0.1mol.�������ᷢ���IJ���������ԭ��Ӧ������D.;���ٷ�Ӧ�����ַ���ʽΪ3Cu��8H����2NO3��=3Cu2����2NO����4H2O������2mol��NO3������2mol�����ᣬ��ͬʱ�ṩ2mol��H+����8mol��H+��������������H+�����ʵ���Ϊ6mol�����С����������3mol����n(H2SO4):n(HNO3)=3:2.��ȷ��
�����Ѷȣ�һ��
2��ѡ���� ����������ײʱ����ȫ�����з�����Ӧ��10NaN3+2KNO3=K2O+5Na2O+16N2���������ж���ȷ����
A����Ӧ��KNO3Ϊ��ԭ��
B��NaN3�е�Ԫ��Ϊ��3��
C����״���£�����6.5gNaN3�μӷ�Ӧ��������3.584L N2
D����1mol KNO���μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ10mol
�ο��𰸣�C
���������A�����ݷ���ʽ��֪������е�Ԫ�صĻ��ϼ۴�+5�۽��͵�0�۵õ����ӣ�������������������A����ȷ��B�����ڻ���������+1�ۣ���˵������е�Ԫ�صĻ��ϼ���-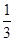 �ۣ�B����ȷ��C��6.5g�����Ƶ����ʵ�����6.5g��65g/mool��0.1mol�����ݷ���ʽ��֪��Ӧ�����ɵ��������ʵ�����0.16mol�����״���µ����������0.16mol��22.4L/mol��3.584L��C��ȷ��D��������е�Ԫ�صĻ��ϼ�+5�۽���0�ۣ��õ�5�����ӣ������1mol KNO���μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ5mol��D����ȷ����ѡC��
�ۣ�B����ȷ��C��6.5g�����Ƶ����ʵ�����6.5g��65g/mool��0.1mol�����ݷ���ʽ��֪��Ӧ�����ɵ��������ʵ�����0.16mol�����״���µ����������0.16mol��22.4L/mol��3.584L��C��ȷ��D��������е�Ԫ�صĻ��ϼ�+5�۽���0�ۣ��õ�5�����ӣ������1mol KNO���μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ5mol��D����ȷ����ѡC��
�����Ѷȣ�һ��
3��ѡ���� С����ʵ��ʱ��С��ճ��һЩ�������,Ƥ���ϳ������ѿ��ĺڰ�,��ʦ�����������ò����ϡ��Һ������ϴ,�䷴Ӧ�����ӷ���ʽΪ:
MnO4��+H2C2O4+H+����������CO2��+Mn2++������(δ��ƽ),����˵������ȷ������������(����ĸ)��?
A���÷�Ӧ��������ΪH2C2O4
B���÷�Ӧ�ұߺ����ϵIJ���ΪOH-
C���÷�Ӧ��ƽ��H+�Ļ�ѧ������Ϊ6
D���ڸ÷�Ӧ����1 mol H2C2O4�μӷ�Ӧ,ת�Ƶ�������Ϊ6NA
�ο��𰸣�C
�����������Ӧ������H+����Ԫ��,������������H2O,���һ����������H2O,B��;��ƽ���ӷ���ʽ:2MnO4��+5H2C2O4+6H+ 10CO2��+2Mn2++8H2O,��1 mol H2C2O4�μӷ�Ӧ,ת�Ƶ�������Ϊ2NA,D��;MnO4��Ϊ������,A����
10CO2��+2Mn2++8H2O,��1 mol H2C2O4�μӷ�Ӧ,ת�Ƶ�������Ϊ2NA,D��;MnO4��Ϊ������,A����
�����Ѷȣ�һ��
4������� ��12�֣�����ѧ�ḻ��ʣ����ڸ�����Ⱥã����������������������棬ͬ��������ɸ������ܵIJ���֡�K2Cr2O7��CrO3�����������ӡȾ�����ϡ���Ƶȹ�ҵ�У��ǹ�ҵ����ɸ���Ⱦ����Ҫԭ���ڱ���ġ������ҡ��¼��У�������Ϊ�ù�ҵƤ����½��ϻ���ƤЬ��Ϊԭ���ƳɵĹ�ҵ������ð���ʳ�������Ƴɽ��ң���ɽ����ڵĸ����س��ꡣ
��1��CrO3�����ȶ��Խϲ����ʱ�ֽ⣬�������������¶ȵı仯��ͼ��ʾ��?
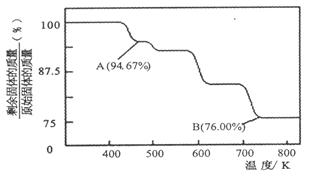
��A ��ʱʣ�����ijɷ���??���ѧʽ����
�ڴӿ�ʼ���ȵ� 750K ʱ�ܷ�Ӧ����ʽΪ?��
��2��Cr(��)��Ҫ��CrO42����Cr2O72����̬���ڣ������������¾��к�ǿ�������ԣ���������Һ�д�������ת����CrO42��(��ɫ)+2H+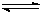 ?Cr2O72��(��ɫ��+H2O��K=4.2��1014����Ҫʹ��Һ�ɻ�ɫ���ɫ����Ӧ��ȡ�Ĵ�ʩ��?��
?Cr2O72��(��ɫ��+H2O��K=4.2��1014����Ҫʹ��Һ�ɻ�ɫ���ɫ����Ӧ��ȡ�Ĵ�ʩ��?��
A����NaOH
B��������
C��������
D����AgNO3