1、选择题 在一定条件下,向饱和的氢氧化钠溶液中加入少量的过氧化钠,充分反应后,恢复原来的温度,下列说法正确的是
[? ]
A.溶液中? 浓度增大,有O2放出?
浓度增大,有O2放出?
B.溶液pH不变,有固体析出,有O2放出?
C.溶液中Na+数目增多,有O2放出?
D.溶液中Na+数目不变,有O2放出
2、填空题 教材中有一个演示实验:用脱脂棉包住约0.2 g Na2O2粉末,置于石棉网上,可观察到脱脂棉燃烧起来。
(1)由实验现象能得出的有关Na2O2与水反应的结论是:a.有氧气生成;b._____________。
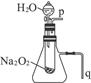
(2)某研究性学习小组拟用如右图所示装置进行实验,以证明上述结论。
①用以验证结论a的实验方法及现象是_____________________________________________。
②用以验证结论b的实验方法及现象是_____________________________________________。
3、填空题 (10分)我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
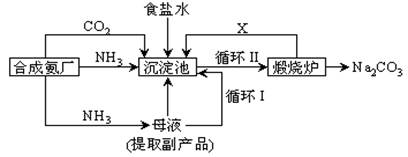
(1) 沉淀池中发生的化学反应方程式是?。
(2) 写出上述流程中X物质的分子式?。
(3)?使原料氯化钠的利用率从70%提高到90%以上,主要是设计了?(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是?。
(4)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加?。
(5) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有?。
(6) CO2是制碱工业的重要原料,目前,常用的两种制碱方法中CO2的来源有何不同??。
4、实验题 (14分)为除去粗盐中的Ca2+. Mg2+. SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
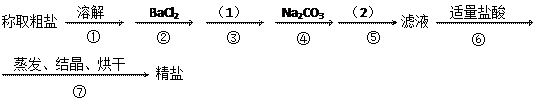
(1)第④步中,写出相应的离子方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
??;? _______________________________
(2)在(1)中应使用除杂试剂的化学式__________,在(2)中的操作名称是_______。
(3)从实验设计方案优化的角度分析步骤 ②和④可否颠倒_
②和④可否颠倒_ ___________(填“是”或“否”,如果“否”,请说明理由。___________________________________________;
___________(填“是”或“否”,如果“否”,请说明理由。___________________________________________;
步骤③和④可否颠倒___________。
(4)若先用盐酸再进行 操作⑤,将对实验
操作⑤,将对实验 结果产生影响,其原因是:
结果产生影响,其原因是:
?
(5)判断BaCl2已过量的方法是?
5、选择题 下列物质放置在空气中因发生氧化还原反应而变质的是(? )
A.氢氧化钠
B.氧化钙
C.过氧化钠
D.氯化钠