1、计算题 室温下,氢氧化钠的溶解度为22 g,将多少克金属钠投入100 g水中,可获得该温度下的饱和溶液。
参考答案:将11.5 g钠投入水中可获得该温度下的饱和溶液。
本题解析:设投入100 g水中的金属钠的质量为x。
2Na+2H2O====2NaOH+H2↑
46? 36? 80? 2
解法1:在一定温度下,饱和溶液中溶质的质量对应100 g溶剂的比值是一常数,建立比例关系。
质量为x的金属钠与质量为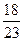 x的水反应,生成质量为
x的水反应,生成质量为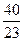 x的氢氧化钠。
x的氢氧化钠。

解得:x="11.5" g
解法2:在一定温度下,饱和溶液的质量分数是常数,由此建立比例关系。
质量为x的金属钠与质量为 的水反应,生成质量为
的水反应,生成质量为 的氢氧化钠,质量为
的氢氧化钠,质量为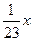 的氢气。
的氢气。

解得:x="11.5" g
解法3:本解法仍是根据饱和溶液中溶质的质量分数是常数建立比例关系,在处理溶液质量时采用简捷的方法,将溶剂和溶入溶剂的反应物的质量总量减去离开溶剂的物质质量(如气体等)。
质量为x的金属钠与水反应生成质量为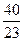 x的氢氧化钠,释放出质量为
x的氢氧化钠,释放出质量为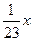 的氢气。
的氢气。

解得:x="11.5" g
本题难度:简单
2、实验题 有人设计了如右图所示实验装置,目的是做钠与水反应的实验并验证:
①钠的物理性质?②钠与水反应的产物是什么
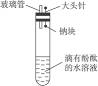
(1)当进行适当操作时还需要的仪器有_________________________________。
(2)如何进行操作?____________________________________。
(3)实验现象是________________________________________。
参考答案:(1)小试管和酒精灯
(2)将大头针向上提,使钠块落入水中,将小试管扣在导管上收集反应产生的气体,用拇指堵住试管口移近酒精灯,松开拇指点燃试管中的气体
(3)钠浮在水面上熔化成闪亮的小球迅速游动,并逐渐消失,水溶液由无色变成红色。点燃小试管中的气体时,有尖锐的爆鸣声。
本题解析:(1)由于实验目的是做Na和水的反应,验证钠的物理性质及证明钠和水的产物是什么,所以要收集产生的气体,并验证气体的可燃性,故还需用小试管和酒精灯。
(2)要由钠和水反应来验证钠的物理性质,使自由的钠块与水接触,就要想办法将钠块放入水中。将大头针向上提,使钠块落入水中,将小试管扣在导管上收集反应产生的气体,用拇指堵住试管口移近酒精灯,松开拇指点燃试管中的气体。
(3)观察到的现象是:钠浮在水面上熔化成闪亮的小球迅速游动,并逐渐消失,水溶液由无色变成红色。点燃小试管中的气体时,有尖锐的爆鸣声。
本题难度:简单
3、选择题 将1 L 1.0 0 mol/L 的Na2CO3溶液逐滴加入到1 L 1.25 mol/L的盐酸中;再做相反操作:将1 L 1.25 mol/L的盐酸逐滴加入1 L 1.00 mol/L 的Na2CO3溶液中,两次操作产生的气体体积之比(同温同压下)是:(?)
A.1∶1
B.2∶1
C.5∶2
D.2∶5
参考答案:C
本题解析:(1)当把碳酸钠加入到盐酸中时由于盐酸相对来说过量,发生反应Na2CO3+2HCl= 2NaCl+H2O+CO2↑。n(HCl)="1.25" mol 所以放出气体0.625 mol 。(2)当把盐酸加入到碳酸钠溶液中时,.碳酸钠与盐酸反应分步进行。首先发生:Na2CO3+HCl= NaHCO3+NaCl;n(Na2CO3)="1.0mol" n(HCl)="1.25" mol消耗盐酸1.0mol.产生NaHCO31.0mol剩余盐酸0.25mol然后发生NaHCO3+HCl= NaCl+H2O+CO2↑。碳酸氢钠对于盐酸来说过量,反应产生的气体按照盐酸来求。盐酸0.25mol,所以产生CO2气体0.25mol。故两次操作产生的气体体积之比为0.625 mol:0.25mol=5:2.选项为 :C。
本题难度:一般
4、计算题 某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
时间/s
| 0
| 5
| 10
| 15
|
读数/g
| 215.2
| 211.4
| 208.6
| 208.6
|
请你据此分析计算:
(1)实验中产生的CO2气体质量为?;
(2)该产品中碳酸钠的质量分数 (结果精确到小数点后一位)?。
参考答案:(1) 6.6克? [2分,未写单位扣1分]?(2) 96.4%?[3分]
本题解析:(1)根据比值数据可知,反应进行到10s时,气体的物质的量不再发生变化,所以CO2的质量是208.6g-215.2g=6.6g。
(2)根据碳原子守恒可知,碳酸钠的质量是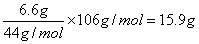 ,则该产品中碳酸钠的质量分数是
,则该产品中碳酸钠的质量分数是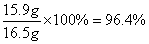
点评:该题是高考中的常见题型和考点,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和规范答题能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
5、选择题 电子工业制造光电管时,需要一种经强光照射就失去电子,从而接通电路的材料。制造这种材料的物质应该是(?)
A.放射性元素
B.超铀元素
C.活泼非金属元素
D.碱金属元素
参考答案:D
本题解析:强光照射就易失去电子的物质应该是活泼的金属单质,答案为D项。
本题难度:简单