1、填空题 ( 13分)西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如下表所示:
?分子式
| 结构简式
| 外观
| 熔点
| 溶解性
|
C12H10ClN3O
| 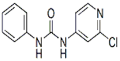
| 白色结晶粉末
| 170~172°C
| 易溶于水
|
(1)氯元素基态原子核外电子的未成对电子数为?。
(2)氯吡苯脲的晶体类型为_______?,所含第二周期元素第一电离能从大到小的顺序为________________。
(3)氯吡苯脲晶体中,氮原子的杂化轨道类型为______?_。
(4)氯吡苯脲晶体中,微粒间的作用力类型有________?_。
A.离子键B.金属键C.共价键D.配位键E.氢键
(5)氯吡苯脲熔点低,易溶于水的原因分别为_________________________________
________________________________________________________________________。
(6)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。
 异氰酸苯酯? 2-氯-4-氨基吡啶?氯吡苯脲
异氰酸苯酯? 2-氯-4-氨基吡啶?氯吡苯脲
反应过程中,每生成1mol氯吡苯脲,断裂_______个σ键、断裂_______个π键
参考答案:(13分)(1)1?(1分)?(2)分子晶体? N> O> C?(各1分,共2分)
(3)sp2、sp3?(各1分,共2分)?(4)C、D?(各1分,共2分)
(5)氯吡苯脲是分子晶体,故熔点低;氯吡苯脲与水分子间形成氢键,故易溶于水。(各1分,共2分)
(6)NA(或6.02×1023)? NA(或6.02×1023)(各1分,共2分)
本题解析:(1)根据构造原理可知,氯元素基态原子核外电子的排布式是1s22s22p63s23p5,所以未成对电子数为1个。
(2)氯吡苯脲的熔点较低,易溶于水,所以其晶体类型是分子晶体。其中所含第二周期元素分别是C、N、O,非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,稳定性强,所以第一电离能大于氧元素的,即正确的顺序是N>O>C。
(3)根据结构简式可知,2个氮原子全部形成单键,属于sp3杂化。另外一个氮原子形成双键,所以是sp2杂化。
(4)氯吡苯脲分子中全部是非金属元素构成的,含有共价键。另外氮原子和氧原子都含有孤对电子,所以还能形成配位键,答案选CD。
(5)由于氯吡苯脲是分子晶体,所以熔点低;另外氯吡苯脲还能与水分子间形成氢键,所以还易溶于水。
(6)由于单键都是σ键、而双键是由1个σ键和1个π键构成的,所以根据反应的方程式可知,每生成1mol氯吡苯脲,断裂NA个σ键和NA个π键。
点评:在判断杂化轨道类型时,应该通过化学键进行,即sp3杂化全部形成单键,sp2杂化中还有1个双键,而sp杂化中还有1个三键。
本题难度:一般
2、选择题 下列物质属于共价化合物的是( )
A.NH4Cl
B.NaCl
C.H2SO4
D.Cl2
参考答案:C
本题解析:
本题难度:一般
3、选择题 使用微波炉加热,具有使受热物质均匀受热、表里一致、速度快、热效率高等优点。其工作原理是通电后炉内的微波场以几亿赫兹的高频改变外电场的方向,水分子因而能迅速摆动,产生热效应,这是因为
[? ]
A.水分子具有极性共价键
B.水分子中有共用电子对
C.水由氢、氧两元素组成
D.水分子是极性分子
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列表示物质结构的化学用语或模型正确的是( )
A.醛基的电子式:
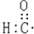
B.丙烷的分子结构的比例模型:
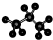
C.乙烯的最简式(实验式):CH2
D.硝基苯的结构简式:
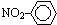
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列说法中,正确的是
A.冰熔化时,分子中H―O键发生断裂
B.原子晶体中,共价键的键长越短,键能越大,熔点就越高
C.分子晶体中,共价键键能越大,该分子的熔沸点就越高
D.分子晶体中,分子间作用力越大,则分子越稳定
参考答案:B
本题解析:冰熔化时,分子中H―O键不变,氢键变化,A不正确;分子晶体中,分子间作用力越强,该分子的熔沸点就越高,C不正确;分子的稳定性和分子间作用力无关系,只与共价键的强弱有关系,D不正确,答案选B。
点评:该题是基础性试题的考查,试题注重基础,侧重能力的培养和解题方法的训练,难度不大。该题有利于培养学生的逻辑推理能力,提高学生发现问题,解决问题的能力。
本题难度:一般