1、选择题 下列性质中,可以证明某化合物内一定存在离子键的是(?)。
A.水溶液能导电
B.由金属和非金属元素的原子组成
C.熔融状态能导电
D.可以溶于水并放出热量
2、填空题 在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量成为键能(kJ?mol-1).下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
| 共价键 | H2分子 | N2分子 | NH3分子
键能(KJ.mo1-1)
436
945
391
|
(1)根据上表中的数据判断工业合成氨的反应是______(填“吸热”或“放热”)反应;
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应.理论上放出或吸收的热量为Q1,则Q1为______.
3、选择题 下列关于共价键的叙述中正确的是
[? ]
A.只有不同种元素的原子之间才能形成共价键
B.由A失去电子,B接受电子的过程形成了共价键
C.原子核外有几个电子就一定能形成几个共价键
D.共用电子对必然偏向吸引电子能力强的一方
4、填空题 【物质结构与性质】(15分)
(1)已知X、Y、Z为同一短周期的三种元素,其原子的部分电离能(kJ/mol)如下表所示:
?
| X
| Y
| Z
|
I1
| 496
| 738
| 577
|
I2
| 4562
| 1451
| 1817
|
I3
| 6912
| 7733
| 2754
|
?
| 9540
| 10540
| 11578
|
①三种元素电负性大小关系为__ _____________
②写出Y原子的电子排布式_____________ Y的第一电离能大于Z的第一电离能的原因_______________________
③X晶体采用下列_________(填字母)堆积方式。
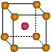 ?
?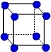 ?
?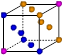 ?
?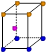
A? B? C? D
(2)N2O的等电子体为:①分子______________,②阴离子______________;由此可知N2O的中心原子的杂化类型为_____________。根据价层电子对互斥模型确定NO2的分子构型为:_____________________________________。
(3)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,
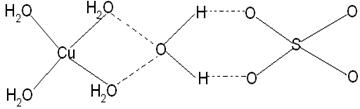
请在图中标出水合铜离子中的配位键.
5、选择题 下列物质中,只含有共价键的是
A.Na2O
B.NaCl
C.HCl
D.NaOH