1、填空题 工业上由银和硝酸反应制AgNO3,在实际生产中,先要把购进的浓HNO3加入等体积的水,稀释后再跟银反应,在加热条件下使反应完成。
试简要完成下列问题。
(1)为什么不直接用浓HNO3,而用稀HNO3和Ag反应制取AgNO3?
(2)该反应放出的尾气为___________,其中___________和___________在空气里会形成黄色或褐色的烟雾,有很大的毒性,这种烟雾通常被称为___________。NO对人体也有很大危害,NO能跟___________作用生成___________而引起中毒。
参考答案:(1)银跟HNO3反应的化学方程式为Ag+2HNO3(浓)====AgNO3+NO2↑+H2O,3Ag+4HNO3(稀)====3AgNO3+NO↑+2H2O。从方程式中可以看出:浓HNO3的利用率为50%,而稀HNO3的利用率为75%,且对空气的污染较小。
(2)NO、NO2? NO? NO2?光化学烟雾?血红蛋白?一氧化氮血红蛋白
本题解析:工业生产一要考虑生产成本,二要考虑环境保护。稀硝酸与银的反应同浓硝酸与银的反应相比,上述两个方面都有优势。
本题难度:简单
2、选择题&nbs p; 下列反应中,属于氮的固定的是(?)
A.空气在雷电的作用下产生NO
B.NH3经催化氧化生成NO
C.NO2和H2O反应生成HNO3
D.由NH3制碳酸铵或硫酸铵
参考答案:A
本题解析:将空气中游离态的氮转化为含氮化合物的过程叫氮的固定。因此,B、C、D都是错误的。故选A。
点评:本题考查的是氮的固定。氮的固定是指将空气中游离态的氮转化为含氮化合物的过程,只要学生学习过程中牢记并理解这些基本定义,便不难解答此题。
本题难度:简单
3、选择题 将5.6 g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入水中,剩余气体的体积为(?)mL
A.1120? B. 2240?C.360? D.4480
参考答案:B
本题解析:略
本题难度:简单
4、实验题 某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是?(用化学方程式表示),所以他认为应该检验?(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。
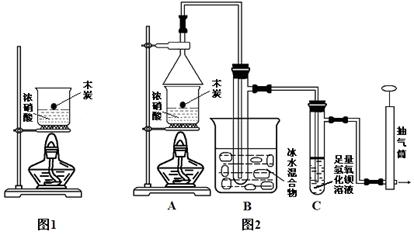
(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)?。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸;?④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用?。
(4)C装置中出现的现象是?,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式?。
参考答案:(1)4HNO3 4NO2↑+O2↑+2H2O(2分)? CO2(1分)
4NO2↑+O2↑+2H2O(2分)? CO2(1分)
(2)④(2分)
(3)常温下存在平衡体系:2NO2 N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。(3分)
N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。(3分)
(4)C中溶液变浑浊(或产生白色沉淀) (3分) 4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O(3分)
本题解析:(1)浓硝酸受热易分解产生二氧化氮气体,4HNO3 4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
(2)只要存在浓硝酸被加热的情况都有可能产生二氧化氮气体,不能证明是C与浓硝酸发生了反应,所以最合理的操作是④;
(3)常温下存在平衡体系:2NO2 N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
(4)若C与浓硝酸反应则有二氧化碳生成,与氢氧化钡溶液反应生成白色沉淀;C的溶液中还含有少量氮元素,只以NO3-形式存在,说明混合气体中仍有NO2,与氢氧化钡溶液、氧气反应生成硝酸钡溶液,化学方程式为4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O。
本题难度:一般
5、选择题 硝酸铜是制备Cu―Zn―Al系催化剂的重要原料。现有三种制取硝酸铜的实验方案可供选用:①铜与稀硝酸反应制取:3Cu + 8HNO3(稀)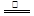 3Cu(NO3)2 + 2NO↑+ 4H2O
3Cu(NO3)2 + 2NO↑+ 4H2O
②铜与浓硝酸反应制取:Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑+ 2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:2Cu + O2 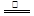 2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O?下列有关说法正确的是(?)
2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O?下列有关说法正确的是(?)
A.制取等量的硝酸铜,需硝酸的量②最少
B.制取等量的硝酸铜,②产生的有毒气体比①少
C.三种方案中,第③方案最经济环保
D.三种方案的反应都可以在铁质容器中进行
参考答案:C
本题解析:A、根据制取硝酸铜的化学反应方程式可以判断:制备1molCu(NO3)2,需要HNO3的物质的量,①中需要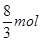 HNO3;②中需要4molHNO3;③中需要2molHNO3,所以需要硝酸的量②>①>③,③最少故A错误;B、由制取硝酸铜三种设计方案的化学反应方程式可以判断:制备1molCu(NO3)2,①中放出
HNO3;②中需要4molHNO3;③中需要2molHNO3,所以需要硝酸的量②>①>③,③最少故A错误;B、由制取硝酸铜三种设计方案的化学反应方程式可以判断:制备1molCu(NO3)2,①中放出 NO气体,②中放出2molNO2气体,③中没有气体放出,制取相同量的硝酸铜①产生的有毒气体比②少,故B错误;C、由制取硝酸铜三种设计方案的化学反应方程式可以判断:制备1molCu(NO3)2,①中需要
NO气体,②中放出2molNO2气体,③中没有气体放出,制取相同量的硝酸铜①产生的有毒气体比②少,故B错误;C、由制取硝酸铜三种设计方案的化学反应方程式可以判断:制备1molCu(NO3)2,①中需要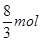 HNO3,放出
HNO3,放出 NO气体,硝酸利用率为
NO气体,硝酸利用率为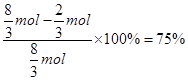 ;②中需要4molHNO3,放出 2molNO2气体,硝酸利用率为
;②中需要4molHNO3,放出 2molNO2气体,硝酸利用率为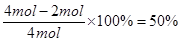 ;③中没有气体放出,HNO3的利用率为100%,三种方案中硝酸的利用率③>①>②,故C正确;D、稀硝酸与铁发生反应,且生成的 Cu(NO3)2?与铁反应,故不可以在铁制容器中进行,故D错误,答案选C。
;③中没有气体放出,HNO3的利用率为100%,三种方案中硝酸的利用率③>①>②,故C正确;D、稀硝酸与铁发生反应,且生成的 Cu(NO3)2?与铁反应,故不可以在铁制容器中进行,故D错误,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型,试题贴近高考,在注重对学生思维能力培养和训练的同时,还注重对学生环境保护意识和能源节约意识的培养,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:一般