1、实验题 “碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表
实验编号
①
②
③
④
⑤
c(I-)/mol・L-1
0.040
0.080
0.080
0.160
0.120
c(SO42-)/mol・L-1
0.040
0.040
0.080
0.020
0.040
t /s
88.0
44.0
22.0
44.0
t2
回答下列问题:
(1)该实验的目的是_______________________。
(2)显色时间t2=_____________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为_____________(填字母)
A <22.0s B 22.0~44.0s C >44.0s D 数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是__________________________
参考答案:(1)研究反应物I-与S2O82-的浓度对反应速率的影响
(2)29.3s
(3)A
(4)反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
本题解析:
本题难度:一般
2、选择题 下列措施中,不能增大化学反应速率的是
A.使用催化剂
B.增大浓度
C.升高温度
D.降低温度
参考答案:D
本题解析:考查外界条件对反应速率的影响。在其它条件下,增大反应物的浓度或升高温度或增大压强或使用催化剂或增大反应物的接触面积或通过原电池反应等都可以增大反应速率。所以答案选D。
本题难度:简单
3、选择题 反应N2O4(g)  2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是? ( )
2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是? ( )
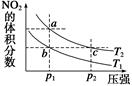
A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a深,c浅
C.b、c两点的平衡常数:b<c
D.a、c两点气体的平均相对分子质量:a>c
参考答案:C
本题解析:A、对于有气体参加的反应,其他条件不变时,增大体系的压强,反应速率加快,所以a<c,错误;B、因为不确定是采用哪种方式增大压强的,所以颜色深浅不确定,错误;C、正确;D、压强增大,平衡左移,所以a<c,错误。
本题难度:一般
4、选择题 用铁片与1 mol・L-1稀硫酸反应制取氢气时,下列措施不能使氢气生成速率增大的是
A.对该反应体系加热
B.加入少量氯化钠固体
C.加入少量3 mol・L-1硫酸
D.不用铁片,改用铁粉
参考答案:B
本题解析:略
本题难度:简单
5、选择题 100毫升12?摩/升盐酸溶液与过量锌粉反应,在一定温度下,为了减慢反应进行的速度,但又不影响生成氢气的总量,可向反应物中加入适量的
①碳酸钙粉末?②氯化钠溶液?③氯化铵(固体)?④水( )
A.①、②
B.①、③
C.②、③
D.②、④
参考答案:①加入碳酸钙粉末,碳酸钙粉末与盐酸反应,降低溶液中H+离子的浓度,但H+离子的总物质的量减小,所以减慢反应进行的速度,但减少影响生成氢气的总量,故①错误;
②加入氯化钠溶液对盐酸进行稀释,降低溶液中H+离子的浓度,且H+离子的总物质的量不变,所以反应速率减慢,但不影响生成氢气的总量,故②正确;
③氯化铵水解溶液呈酸性,增大了溶液中H+离子的浓度,且H+离子的总物质的量增大,所以加快反应进行的速度,也增加影响生成氢气的总量,故③错误;
④加入水对盐酸进行稀释,降低溶液中H+离子的浓度,且H+离子的总物质的量不变,所以反应速率减慢,但不影响生成氢气的总量,故④正确;
故选:D.
本题解析:
本题难度:简单