1、简答题 ①在标准状况下,112mL某气体的质量是0.14g,则其相对分子质量为______.
②含有相同原子个数的SO2和SO3,其质量比为______,摩尔质量比为______,
③200mL2.00mol/L的Al2(SO4)3溶液中含有______mol?Al2(SO4)3,Al3+的物质的量浓度为______mol?L-1,含Al3+的质量为______g.
参考答案:①n=0.112L22.4L/mol=0.005mol,M=mn=0.14g0.005mol=28g/mol,则相对分子质量为28,故答案为:28;
②假设原子个数为N,则n(SO2)=13×NNAmol,n(SO3)=14×NNAmol,
m(SO2):m(SO3)=13×NNAmol×64g/mol:14×NNAmol×80g/mol=16:15;
M(SO2):M(SO3)=64g/mol:80g/mol=4:5,
故答案为:16:15;4:5;
③n(Al2(SO4)3)=0.2L×2.00mol/L=0.40mol;
n(Al3+)=2n(Al2(SO4)3)=0.80mol,
c(Al3+)=2c(Al2(SO4)3)=4.00mol/L;
m(Al3+)=0.80mol×27g/mol=21.6g,
故答案为:0.40;4.00;21.6.
本题解析:
本题难度:一般
2、填空题 (2分)将质量分数为98%,密度为1.84 g・cm-3的浓硫酸,用蒸馏水稀释到9.2 mol/L的硫酸,则其质量分数?49%(填>、<、=)。
参考答案:>
本题解析:因为硫酸溶液的密度是随浓度的增大而增大的,所以根据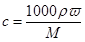 可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
本题难度:一般
3、选择题 0.5L 1mol・L―1 FeCl3溶液与0.2L 1mol・L―1 KCl溶液中的Cl―的物质的量浓度之比
A.5∶2
B.3∶1
C.15∶2
D.1∶3
参考答案:B
本题解析:略
本题难度:一般
4、填空题 100mL 1 mol/LAl2(SO4)3溶液中,Al3+物质的量浓度是 ,含Al3+物质的量 mol,从其中取10ml,Al2(SO4)3物质的量浓度是 ,再将这10ml溶液稀释成100ml,物质的量浓度又为 。Al3+与SO42-物质的量浓度之比是 。
参考答案:2mol/L,0.2mol,1mol/L,0.1mol/L,2:3.
本题解析: 铝离子浓度为1mol/L×2=2mol/L,含有的铝离子的物质的量为2mol/L×0.1L=0.2mol,从其中取出一部分,物质的量浓度不变,是1mol/L,将溶液稀释后浓度为1mol/L×0.01L÷0.1L=0.1mol/L,铝离子和硫酸根的浓度比等于2:3.
考点:物质的量浓度的计算。
本题难度:一般
5、选择题 某种气体的摩尔质量为M g・mol-1,将标况下的该气体V L溶解在1000 g水中,该气体不与水反应,所得溶液密度为ρ g・cm-3,则所得溶液中溶质的物质的量浓度为 (? ) mol・L-1
A.V/22.4
B.V ρ/(MV+22400)
C.V ρ/22400
D.1000V ρ/(MV+22400)
参考答案:D
本题解析:该溶液的质量为: ,所以该溶液的体积为:
,所以该溶液的体积为: ,再由物质的量浓度的概念:
,再由物质的量浓度的概念: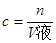 代入得,所得溶液中溶质的物质的量浓度为1000V ρ/(MV+22400);
代入得,所得溶液中溶质的物质的量浓度为1000V ρ/(MV+22400);
本题难度:一般