1�������� ��13�֣���25��ʱ���������ʵ�����A��B�����2L���ܱ������У��������з�Ӧ��3A��g��+B(g) 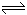 xC(g)+2D(g) ����H>0����5min���֪D��Ũ��Ϊ0.5mol/L��
xC(g)+2D(g) ����H>0����5min���֪D��Ũ��Ϊ0.5mol/L��
A��B�����ʵ���Ũ��֮��Ϊ3:5��C��ƽ����Ӧ������0.1mol/(L��min)����
��1����ʱA�����ʵ���Ũ����?��
��Ӧ��ʼǰ�����е�A��B�����ʵ�����n(A)= n(B)=??
��2��x��ֵΪ?��5min��B��ƽ����Ӧ����?��
��3�����д�ʩ��ʹ����Ӧ�����������?��������ѡ��
A. ֻ����A��Ũ��? B.����Ӧ���¶�
C. ��������ͨ��һ�������He������Ӧ��ѹǿ? D. ʹ�ô���
��4��������3L���ܱ�������ʢ����������ͬ����A��B���壬��ﵽƽ���A��B�����ʵ���Ũ�ȵı�ֵ?3:5���>����=����<������
�ο��𰸣���13�֣���1��0.75mol/L? 3mol?��2��0.05mol/(L��min)? 2
��3�� ABD?��4��=
���������������淴Ӧ���йؼ��㼰��������Է�Ӧ���ʺ�ƽ���Ӱ�졣
��1��C��ƽ����Ӧ������0.1mol/(L��min)����C��Ũ����0.5mol/L�����Ը��ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪x��2������Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����B�ķ�Ӧ������0.1mol/(L��min)��2��0.05mol/(L��min)��
��2��? 3A��g��+B(g) 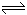 2C(g)+2D(g)
2C(g)+2D(g)
��ʼ����mol��? n? n? 0? 0
ת������mol��? 1.5? 0.5? 1.0? 1.0
ƽ������mol��? n��1.5? n��0.5? 1.0? 1.0
������n��1.5���U��n��0.5���� 3:5
���n��3mol������A��Ũ����1.5mol��2L��0.75mol/L
��3���������������������£�����Ӧ��Ũ�Ȼ������¶Ȼ�����ѹǿ��ʹ�ô����Ⱦ��ܼӿ췴Ӧ���ʣ�ѡ��C��Ũ�Ȳ��䣬��Ӧ���ʲ��䣬���Դ�ѡABD��
��4����Ϊ��Ӧǰ��������䣬���Դ�ʱ��ƽ���ǵ�Ч�ģ���˱�ֵ���䡣
�����Ѷȣ�һ��
2��ѡ���� �ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣�����ܱ������еķ�Ӧ��N2(g)+3H2(g) 2NH3(g)?Ϊ���ȷ�Ӧ��400�� 30 MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ����
2NH3(g)?Ϊ���ȷ�Ӧ��400�� 30 MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ����
A����a���淴Ӧ���ʱȵ�b�Ĵ�
B����c����Ӧ�ﵽƽ��
C����d(t1ʱ��)�͵�e(t2ʱ��)��n(N2)��һ��
D����d(t1ʱ��)�͵�e(t2ʱ��)��H2��ת������ͬ
�ο��𰸣�D
�������������ͼ���֪��a���������Ũ��С��b���������Ũ�ȣ������淴Ӧ����С��b�㣬A����ȷ��C�����ʵ�Ũ����Ȼ�DZ仯�ģ�����ƽ��״̬��B����ȷ��d��e�����������ͬ�����µ�ƽ��״̬�����Ե��������ʵ�������ͬ�ģ�ת����Ҳ����ͬ�ģ�C����ȷ��D��ȷ����ѡD��
�����Ѷȣ�һ��
3�������� ��һ�������£����淴ӦA2(g)��B2(g)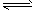 2C(g)��һ���ݻ��̶����ܱ������дﵽƽ��ʱ�����
2C(g)��һ���ݻ��̶����ܱ������дﵽƽ��ʱ�����
c(A2)=0��5mol��L-1�� c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1����A2��B2��C����ʼŨ�ȷֱ�Ϊ
amol��L-1��b mol��L-1��gmol��L-1��ȷ����
��1��a��gӦ����Ĺ�ϵʽΪ_________��
��2������Ӧ������Ӧ����ʼ���У���g��_________��a�����ֵΪ_________��
��3������Ӧ���淴Ӧ����ʼ���У���b��_________��a����СֵΪ_________��
��4��b��ȡֵ��ΧΪ________________��
�ο��𰸣���1��a+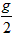 =1.3
=1.3
��2��0��1.3
��3��0��0.4
��4��0��b��0.9
���������
�����Ѷȣ�һ��
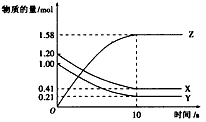
4��ѡ���� һ���¶��£���2L ���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯����������ͼ��ʾ������������ȷ����
[? ]
A����Ӧ��ʼ��10 s����Z��ʾ�ķ�Ӧ����Ϊ0.158 mol��L-1��s-1
B����Ӧ��ʼ�� l0 s��X�����ʵ���Ũ�ȼ�����0.79 mol��L-1
C����Ӧ��ʼ��10 s��Y��ת����Ϊ79.0%
D����Ӧ�Ļ�ѧ����ʽΪ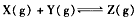
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� һ���¶��£���Ӧ2SO2+O2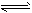 2SO3�ﵽƽ��ʱ��n(SO2)�Un(O2) �Un(SO3) ===2�U3�U4����С�������Ӧ�ٴδﵽƽ��ʱ��n(O2) =0.8mol��n(SO3)=1.4mol����ʱSO2�����ʵ���Ӧ��
2SO3�ﵽƽ��ʱ��n(SO2)�Un(O2) �Un(SO3) ===2�U3�U4����С�������Ӧ�ٴδﵽƽ��ʱ��n(O2) =0.8mol��n(SO3)=1.4mol����ʱSO2�����ʵ���Ӧ��
[? ]
A.0.4mol
B.0.6mol
C.0.8mol
D.1.2mol
�ο��𰸣�A
���������
�����Ѷȣ�һ��