1、选择题 在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g);ΔH =QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g);ΔH =QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
 ? ?
温度℃
| 1
| 2
| 3
|
100
| 1.00
| 0.75
| 0.53
|
200
| 1.20
| 0.09
| 0.63
|
300
| 1.30
| 1.00
| 0.70
|
下列说法正确的是
A.m>n? B. 温度不变,压强增大,Y的质量分数减少
C. Q<0?D.体积不变,温度升高,平衡向逆反应方向移动
参考答案:B
本题解析:根据表中数据可知,在体积相同的条件下,温度越高Y的物质的量浓度越大,这说明升高温度有利于Y的生成,因此正方应是吸热反应,即Q>0;在温度相同的条件下,气体的体积越大,Y的物质的量浓度越小。这说明增大压强,不利于Y的生成,即正方应是体积增大的可逆反应,所以m<n,因此选项ACD都是错误的,答案选B。
点评:该题是中等难度的试题,试题综合性强,在注重对学生基础知识巩固和系列的同时,侧重对学生能力的培养和解题方法的指导与训练。旨在培养学生灵活运用基础知识解决实际问题的能力,有利于调动学生的学习兴趣,激发学生的学习求知欲。
本题难度:简单
2、选择题 在某恒定温度下,向容积为1 L的容器中投入1 mol CO和2 mol H2O,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),平衡时生成CO2 2/3 mol。若保持温度和容积不变,向其中增加2 mol H2O(g),使反应到达新的平衡,下列说法不正确的是(?)
A.新、旧平衡时容器内气体的压强之比是5:3
B.新平衡时H2O的转化率为20%
C.新平衡时CO的浓度是0.2 mol ・L-1
D.新、旧平衡时容器内气体密度之比为5:3
参考答案:D
本题解析:略
本题难度:一般
3、填空题 在体积为2 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
T/℃
| 700
| 800
| 850
| 1 000
| 1 200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
?
回答下列问题:
(1)Q____0(填 “>”、“<”),升高温度,化学平衡向________(填“正反应”或“逆反应”)方向移动。
(2)若某温度下,平衡浓度符合下列关系:c(CO2)・c(H2)=c(CO)・c(H2O),此时的温度为__________;在此温度下,若该容器中含有1mol CO2、3mol H2、2mol CO、2mol H2O,则此时反应所处的状态为____________(填“向正反应方向进行中”、“向逆反应方向进行中”或“平衡状态”),此温度平衡时CO2的浓度为___________ mol・L-1;在此温度下,若该容器中含有1.5mol CO2、3.5mol H2、1.5mol CO、1.5mol H2O达到平衡时CO2的浓度为___________ mol・L-1。
参考答案:(1)?>(1分)?正反应(1分)?
(2)850 ℃(2分) ?向逆反应方向进行中(2分)? 0.56(2分)? 0.56(2分)
本题解析:(1)升高温度,K变大,说明反应为吸热反应。(2)因为c(CO2)・c(H2)=c(CO)・c(H2O),可以推出K=1,则温度为)850 ℃。带入Q的运算公式,发现Q>1,平衡逆移。列出平衡时刻各浓度,带入K公式,可以求出变化量,即可求出CO2的浓度。投料为1.5mol CO2、3.5mol H2、1.5mol CO、1.5mol H2O时,相当于投料为1mol CO2、3mol H2、2mol CO、2mol H2O,则构成相同的平衡。
本题难度:一般
4、选择题 已知某可逆反应aA(g) + bB(g)  ?cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的
?cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的
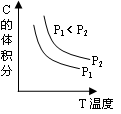
A.正反应为吸热反应
B.降低温度,正反应速率增大
C.a + b < c + d
D.增大压强,B转化率增大
参考答案:D
本题解析:根据图像可知,随着温度的升高,C的体积分数降低。说明升高温度平衡向逆反应方向移动,因此正反应是放热反应,A不正确;降低温度,反应速率一定是减小的,B不正确;当温度相同时,压强越大,C的体积分数越大。说明增大压强,平衡向正反应方向移动,即正反应是体积减小的,所以C不正确,D正确,答案选D。
本题难度:简单
5、选择题 在容积不变的密闭容器中加入1 mol N2和3 mol H2发生反应,下列叙述正确的是

A.该反应的热化学方程式为:N2 + 3H2 2NH3ΔH =-92 kJ/mol
2NH3ΔH =-92 kJ/mol
B.达到平衡后向容器中通入1 mol氦气,平衡不移动
C.曲线b表示可能使用了催化剂
D.降低温度和缩小容器体积均可使该反应平衡常数增大
参考答案:BC
本题解析:A、热化学方程式中应该在反应物与生成物的后边标明物质的聚集状态,错误;B、达到平衡后向容器中通入1 mol氦气,因为体积是固定的,不影响各种物质的浓度,因此各种物质的速率不变,从而平衡不移动,正确;C、正确;D、该平衡正向是一个放热反应,降低温度时,平衡正向移动,增大了平衡常数,缩小体积时,因为温度不变,因而平衡常数不变,错误。
本题难度:一般