1、填空题 (6分)下列10种物质中:①NaOH溶液②H2SO4③硫酸铜晶体④Cu ⑤CH3COOH?⑥NaOH固体⑦蔗糖⑧石灰水⑨水银⑩氨水
能导电的有?;属于强电解质的有?;属于弱电解质的有?。
参考答案: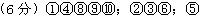
本题解析:略
本题难度:简单
2、选择题 向体积相同,pH为1的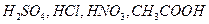 溶液中,分别加入足量的金属镁,下列说法中不正确的是(?)
溶液中,分别加入足量的金属镁,下列说法中不正确的是(?)
A.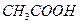 产生的H2最多
产生的H2最多
B.HNO3产生的H2最少
C.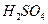 和HCl产生的H2一样多
和HCl产生的H2一样多
D.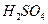 产生的H2比HCl产生的H2多
产生的H2比HCl产生的H2多
参考答案:D
本题解析:略
本题难度:简单
3、简答题 25℃时,硫氢化钾溶液里存在下列平衡:
a、HS-+H2O?OH-+H2S
b、HS-?H++S2-
①当向其中加入硫酸铜溶液时,生成了CuS沉淀,则电离平衡向______移动;水解平衡向______移动;c(H+)变______(填“大”或“小”).
②当向其中加入氢氧化钠固体时,c(S2-)变______(填“大”或“小”).
参考答案:①向其中加入硫酸铜溶液时,生成了CuS沉淀,S2-浓度减小,促进HS-的电离,电离平衡向右移动,溶液中H+的浓度增大,HS-浓度减小,水解平衡向左移动,水解程度减小,
故答案为:右;左;大;
②当向其中加入氢氧化钠固体时,发生:H++OH-=H2O,促进HS-的电离,平衡向正方向移动,c(S2-)变大,
故答案为:大.
本题解析:
本题难度:一般
4、选择题 常温下,pH=12的氨水中存在以下电离平衡:
NH3・H2O NH4+ +OH-。往其中加入少量0.01 mol・L-1NaOH溶液,保持不变的是(? )
NH4+ +OH-。往其中加入少量0.01 mol・L-1NaOH溶液,保持不变的是(? )
A.c(NH4+)
B.c(OH-)
C.c(NH3・H2O)
D.c(NH4+)・c(OH-)
参考答案:B
本题解析:pH=12的氨水中c(OH-)=10-2 mol・L-1,故再加入等浓度的NaOH溶液,c(OH-)不会改变;由于溶液体积变大,故c(NH4+)、c(NH3・H2O)、c(NH4+)・c(OH-)都会变小,故A、C、D错误
本题难度:一般
5、选择题 用水稀释 时,溶液中随着水量的增加而减小的是
时,溶液中随着水量的增加而减小的是
A.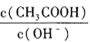
B.
C.c(H+)和c( OH-)的乘积
D.OH-的物质的量
参考答案:A
本题解析:A.加水稀释促进酸电离,氢离子浓度、酸浓度、酸根离子浓度都降低,但氢离子浓度减小的量小于酸分子减小的量,所以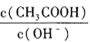 减小,故A正确;
减小,故A正确;
B.加水稀释促进酸电离,酸浓度、酸根离子浓度都降低,但酸根离子浓度减小的量小于酸分子减小的量,所以氢氧根离子浓度增大,则 增大,故B错误;
增大,故B错误;
C.温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,故D错误;
故选A。
点评:本题考查了弱电解质的电离,易错题,注意加水稀释时溶液中各种微粒浓度的变化,虽然促进弱电解质电离,但加入水的量远远大于弱电解质电离的量,为易错点。
本题难度:一般