1、选择题 室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中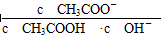 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
2、填空题 已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH)?l.8 xl0-5,Ka(HSCN)?0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图。
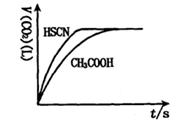
反应开始时,两种溶液产生CO2的速率明显不同的原因是?;
反应结束后所得溶液中c(SCN-)____?c(CH3COO-)(填“>”,“=”或“<”)。
(2)2.0×l0-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如下图。

则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=?
(3)难溶物质CaF2溶度积常数为:Ksp= 1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4 mol/L的CaCl2溶液等体积混合,调节溶液pH =4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?____?(填“有”或“没有”),筒述理由:?。
3、填空题 (Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
实验
编号
| HA的物质的量浓度(mol・L-1)
| NaOH的物质的量浓度(mol・L-1)
| 混合后溶液的pH
|
甲
| 0.1
| 0.1
| pH=a
|
乙
| 0.12
| 0.1
| pH=7
|
丙
| 0.2
| 0.1
| pH>7
|
丁
| 0.1
| 0.1
| pH=10
|
?
(1)从甲组情况分析,如何判断HA是强酸还弱酸?
?。
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是?。
A.前者大?B.后者大? C.二者相等 ?D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是?。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=??mol/L。
(Ⅱ)某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB- H++B2-
H++B2-
回答下列问题:
(5)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是?。
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
4、选择题 已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH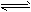 CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
[? ]
A.加少量烧碱
B.降低温度
C.加少量冰醋酸
D.加水
5、简答题 以下说法中正确的是( )
A.pH=2的酸溶液稀释100倍后溶液的pH=4
B.c(NH4+)相等的(NH4)2SO4溶液与(NH4)2S溶液中:c[(NH4)2SO4]<c[(NH4)2S]
C.25℃时纯水的pH低于100℃时纯水的pH
D.pH=3的硫酸物质的量浓度是pH=3的醋酸物质的量浓度的0.5倍