| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《原电池原理》答题技巧(2019年最新版)(二)
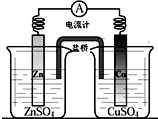 参考答案:该原电池中,锌的活泼性大于铜,所以锌作负极,铜作正极;正极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu;负极上锌失电子生成锌离子进入溶液,所以锌片逐渐溶解;外电路中,电子从负极锌沿导线流向正极铜;盐桥中的阴离子向硫酸锌溶液中迁移,阳离子向硫酸铜溶液中迁移. 本题解析: 本题难度:简单 5、选择题 LiFePO4可用于电动汽车.电池反应为:FePO4+Li A.该电池可用水作电解质溶液 B.充电时,电池内部的Li+向阳极移动 C.充电阳极反应LiFePO4-e-=FePO4+Li+ D.放电时正极材料的质量减少 参考答案:A.放电时金属锂做负极,锂可与水发生反应,故A错误; 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《原子核外电.. | |