1、选择题 下列有关化学反应过程或实验现象的结论中,正确的是( )。
A.NH3的水溶液可以导电,说明NH3是电解质
B.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si
C.在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液,溶液褪色,说明CaCl2
溶液显酸性
D.向淀粉碘化钾溶液中加入溴水,溶液变为蓝色,说明Br2的氧化性强于I2
参考答案:D
本题解析:NH3与水反应生成的NH3・H2O能电离出自由移动的离子,而NH3属于非电解质;由反应2C+SiO2 2CO↑+Si可得高温下C的还原性强于Si;D项中发生的反应为2KI+Br2=2KBr+I2,即Br2的氧化性强于I2。
2CO↑+Si可得高温下C的还原性强于Si;D项中发生的反应为2KI+Br2=2KBr+I2,即Br2的氧化性强于I2。
本题难度:一般
2、选择题 短周期元素W、X、Y、Z在元素周期表中的位置关系如图所示。下列说法正确的是

[? ]
A.元素Y的最高价氧化物对应水化物的酸性比Z的 强
B.元素Z位于元素周期表的第3周期VIIA族
C.原子半径的大小顺序为:rY>rW>rX
D.元素X可能为硼或碳或氮
参考答案:D
本题解析:
本题难度:一般
3、选择题 几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是
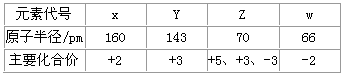
[? ]
A.X、Y元素的金属性X Y
Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
参考答案:D
本题解析:
本题难度:简单
4、填空题 现有部分短周期元素的性质或原子结构如下表

(1)写出B元素在元素周期表中的位置_______________。
(2)写出C元素气态氢化物的电子式_______________。
(3)元素D与元素B相比,非金属性较强的是____________(用元素符号表示),下列叙述中能证明这一事实的是_______________(填数字序号)。
① 常温下D的单质和B的单质状态不同
② D的气态氢化物比B的气态氢化物稳定
③ B元素最高价氧化物的水化物酸性强于D元素最高价氧化物的水化物酸性
(4)由表中元素形成的常见物质X、Y、Z、M、N存在以下转化关系:
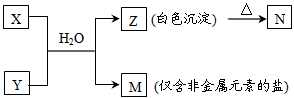
①N的化学式为_________________。
②X溶液与Y溶液反应的离子方程式为___________________________。
参考答案:(1)第三周期第ⅥA族
(2)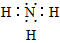
(3)Cl;②
(4)①Al2O3;②Al3++3NH3・H2O==Al(OH)3↓+3NH4+
本题解析:
本题难度:困难
5、推断题 A-F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示

请回答下列问题:
(1)A在元素周期表中的位置是___________;A与E形成的化合物的电子式是___________。
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是_____________________________。
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是___________________。
(4)F的盐酸盐水溶液呈酸性,原因是___________________(用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是____________________。
(5)A与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中A元素的含量。(装置中因空气质量引起的误差忽略不计)
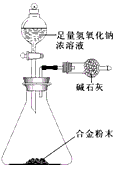
①实验需要测定三个物理量:合金的质量m以及a和b。a是_______;b是________。
②合金中A元素的质量分数是___________(用含m、a、b的式子表示)。
参考答案:(1)第3周期,ⅡA族;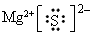
(2)2Fe3+ + Cu == 2Fe2+ + Cu2+
(3)C + H2O CO + H2
CO + H2
(4)Al3+ + 3H2O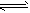 Al(OH)3 + 3H+;2Al + Fe2O3
Al(OH)3 + 3H+;2Al + Fe2O3 2Fe + Al2O3
2Fe + Al2O3
(5)①反应前装置和药品的总质量;反应后装置和药品的总质量;②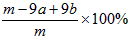
本题解析:
本题难度:困难