1��ѡ���� �������������ܿ϶��ж�ij��ѧƽ�ⷢ���ƶ�����(����)
A��������и���ֵ�Ũ�ȸı�
B�������ϵ�������ܶȷ����仯
C�������淴Ӧ���ʸı�
D����Ӧ���ת���ʸı�
�ο��𰸣�D
�����������I2(g)+H2(g)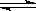 2HI(g)�����ϵ��ѹ��ƽ�ⲻ�ƶ���������ֵ�Ũ�ȶ�����������ܶȱ�����淴Ӧ���ʱ������A��B��C���Ǵ���ģ���Ӧ���ת���ʸı䣬ƽ��һ���ƶ���D��ȷ����ѡD��
2HI(g)�����ϵ��ѹ��ƽ�ⲻ�ƶ���������ֵ�Ũ�ȶ�����������ܶȱ�����淴Ӧ���ʱ������A��B��C���Ǵ���ģ���Ӧ���ת���ʸı䣬ƽ��һ���ƶ���D��ȷ����ѡD��
������������Ũ�ȡ�ѹǿ���ܶȵȸı����ж�ƽ���ƶ�����Ӧ����ת���ʡ���������ĸı����ж�ƽ����ƶ���
�����Ѷȣ�һ��
2��ѡ���� ��2L�ܱ������У�����X��Y��4mol��һ�������·�����ѧ��Ӧ��2X��g��+ 2Y��g�� Z��g��+2 W��g����H<0����Ӧ���е�5sʱ���X��ת����Ϊ25%��10 s��ﵽ��ѧƽ�⣬���Z��Ũ��Ϊ0.5mol/L��������˵����ȷ����
Z��g��+2 W��g����H<0����Ӧ���е�5sʱ���X��ת����Ϊ25%��10 s��ﵽ��ѧƽ�⣬���Z��Ũ��Ϊ0.5mol/L��������˵����ȷ����
A��5s��ƽ����Ӧ����Ϊ��(Y)=" 0.2" mol/( L��s)
B���÷�Ӧ��ƽ�ⳣ����ֵΪ0.5
C�������ݻ�������䣬��������ͨ������������߷�Ӧ���ת����
D�������¶ȣ�������������ܶȲ���ʱ����ʾ�÷�Ӧ�Ѿ��ﵽƽ��״̬
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
3��ѡ���� ����ѹǿ��ʹ���л�ѧ��Ӧ��ƽ��������Ӧ�����ƶ����ǣ�?����
A��C(s)+CO2(g) 2CO(g)
2CO(g)
B��3H2(g)+N2(g) 2NH3(g)
2NH3(g)
C��H2(g)+I2(g) 2HI(g)
2HI(g)
D��C(s)+H2O(g) CO(g) + H2(g)
CO(g) + H2(g)
�ο��𰸣�B
���������Ҫʹ����ѹǿ����ѧ��Ӧ������Ӧ�����ƶ���������Ӧ����Ϊ����������ٵķ����ƶ���������ȷѡ��ΪB��
�����Ѷȣ���
4��ѡ���� ���ܱ����з������з�ӦaA(g)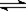 cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ���� (? )
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ���� (? )
A��A��ת���ʱ��
B��ƽ��������Ӧ�����ƶ�
C��D������������
D��a �� c��d
�ο��𰸣�D
������������������ѹ����ԭ����һ��˲��D��Ũ����������2�������ﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8����˵������ѹǿƽ�����淴Ӧ�����ƶ������a �� c��d��������ȷ�Ĵ�ѡD��
�����Ѷȣ���
5��ѡ���� ��373K?ʱ����0.5mol?N2O4����ͨ�����Ϊ5L������ܱ������У��������ֺ���ɫ��N2O4?2NO2����Ӧ���е�2sʱ��NO2��Ũ��Ϊ0.02mol/L����60sʱ����ϵ�Ѵﵽƽ�⣬��ʱ������ѹǿΪ��Ӧǰ��1.6��������˵����ȷ���ǣ�������
A��ǰ2?s����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01?mol?L-1?s-1
B��ƽ��ʱ�����������ڳ�������������壬������N2O4��ת����
C��ƽ��ʱ����ϵ�ں�N2O4?0.25?mol
D����2?sʱ����ϵ��ѹǿΪ��Ӧǰ��1.1��
�ο��𰸣�A.2��ʱ��NO2��Ũ��Ϊ0.02Ħ/������ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ�ٶ�Ϊ0.01mol/L2s=0.005mol/L��s����A����
B��ƽ��ʱ�����������ڳ�������������壬�൱����ԭ���Ļ�������С�������N2O4�T2NO2������С�����ѹǿ����ѧƽ�������ƶ���N2O4��ת���ʽ��ͣ���B����
C����ת����N2O4�����ʵ���Ϊx����ƽ��ʱN2O4�����ʵ���Ϊ0.5mol-x��NO2�����ʵ���Ϊ2x����ƽ��ʱ������ѹǿΪ��ʼʱ��1.6������0.5mol-x+2x0.5mol=1.6�����x=0.3mol����ƽ��ʱN2O4�����ʵ���Ϊ0.5mol-x=0.5mol-0.3mol=0.2mol����C����
D����N2O4�T2NO2��2��ʱNO2�����ʵ���Ϊ0.1mol��N2O4�����ʵ���Ϊ0.5mol-0.01mol/L��5L=0.45mol���ɷ�Ӧǰ������ʵ���֮�ȵ���ѹǿ֮�ȣ�����2��ʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��0.1mol+0.45mol0.5mol=1.1������D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��