1��ѡ���� һ�������£��ڷ�Ӧ2SO2��g��+O2��g��?2SO3��g��ƽ����ϵ�У�n��SO2��=2.0mol/L��n��O2��=0.8mol/L��n��SO3��=2.4mol/L����SO2����ʼŨ�ȵķ�ΧΪ��������
A��0.4��2.0mol/L
B��0.4��4.4mol/L
C��0��4mol/L
D����ȷ��
�ο��𰸣���������Ӧ���н���ƽ�⣬�����������ʼŨ��������������Ũ�ȱ仯��Ϊ��n��SO3��=2.4mol/L���ɷ���ʽ2SO2��g��+O2��g��?2SO3��g�����������Ũ�ȱ仯����n��SO2��=��n��SO3��=2.4mol/L���ʶ����������ʼŨ�ȼ���ֵΪ2mol/l+2.4mol/L=4.4mol/L��
�����淴Ӧ��ʼ����ƽ�⣬�����������ʼŨ����С���ɷ���ʽ2SO2��g��+O2��g��?2SO3��g����֪�����ɵĶ���������������Ũ�ȱ仯��֮��Ϊ2��1��ʵ��Ϊ2mol/L��0.8mol/L=2.5��1���ʿ�ʼ���������Ũ�Ȳ�Ϊ0����������Ũ�ȿ�֪ת�����ɵĶ�������Ũ��Ϊ0.8mol/L��2=1.6mol/L���ʶ����������ʼŨ�ȼ�СֵΪ2mol/L-1.6mol/L=0.4mol/L��
�ʶ����������ʼŨ�Ƚ���0.4��4.4mol/L֮�䣬
��ѡB��
���������
�����Ѷȣ�һ��
2��ѡ���� �����������ڶ��������·���ˮ�ⷴӦ��CH3COOC2H5��H2O CH3COOH��C2H5OH��֪�÷�Ӧ��������c(H��)��������ӿ졣ͼΪCH3COOC2H5��ˮ��������ʱ��ı仯ͼ������˵������ȷ����(����)
CH3COOH��C2H5OH��֪�÷�Ӧ��������c(H��)��������ӿ졣ͼΪCH3COOC2H5��ˮ��������ʱ��ı仯ͼ������˵������ȷ����(����)

A����Ӧ����ˮ�����������������Һ��c(H��)����������
B��A��B�����ʾ��c(CH3COOC2H5)���
C��ͼ��t0ʱ��Ӧ�ﵽƽ��״̬
D��tBʱCH3COOC2H5��ת���ʵ���tAʱCH3COOC2H5��ת����
�ο��𰸣�A
����������ոշ�Ӧ��ʼ��ʱ����������ˮ��������ᣬ������������Ӳ������ӣ���Ӧ���ʲ��ϼӿ졣���ŷ�Ӧ�Ľ��У�����������Ϊ��Ӧ�Ũ�Ȳ��ϼ��٣���ʱ��Ӧ���ʿ�ʼ���͡�
A���ոշ�Ӧ��ʼ��ʱ����������ˮ��������ᣬ������������Ӳ������ӣ���Ӧ���ʲ��ϼӿ죬��A��ȷ��B��B���A����ȣ�����ˮ������������࣬��A��B�����ʾ��c��CH3COOC2H5��A�����B�㣬��B����C��ͼ��toʱ��ʾ��������ˮ���������û�дﵽƽ��״̬����C����D������������Ϊ��Ӧ�ﲻ�ϼ��٣����tBʱCH3COOC2H5��ת���ʸ���tAʱCH3COOC2H5��ת���ʣ���D����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ӱ�������ǿ��ע�ش��������� ������������ѧ�������������������Ӧ�������������ڼ���ѧ����ѧϰ�����ԡ�����ʱע�����ͼ�����Ӱ�������Լ����ʱ仯�ص㡣
�����Ѷȣ�һ��
3������� ��5�֣�
��2L�ܱ�������ͨ��amol����A��bmol����B����һ�������·�����Ӧ��
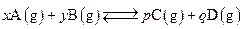
��֪��ƽ����Ӧ����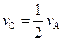 ����Ӧ2minʱ��A��Ũ�ȼ�����
����Ӧ2minʱ��A��Ũ�ȼ����� ��B�����ʵ���������
��B�����ʵ���������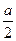 mol����amolD���ɡ�
mol����amolD���ɡ�
�ش��������⣺
��1����Ӧ2min�ڣ� =��
=�� ��
��
��2����ѧ����ʽ�У�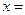 ��
��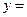 ��
��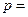 ��
�� ��
��
��3����Ӧƽ��ʱ��DΪ2amol����B��ת����Ϊ��
��4�����ֻ���߷�Ӧ�¶ȣ�������Ӧ�������䣬ƽ��ʱDΪ1.5amol����÷�Ӧ��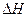
0�����������������������
��5����������������䣬���������ݻ���Ϊ1L������ͬ����ʵ�飬����������Ӧ�Ƚϣ�
�ٷ�Ӧ���ʣ����������С�����䡱���������ǣ�
��ƽ��ʱ��Ӧ���ת���ʣ����������С�����䡱���������ǣ�
�ο��𰸣�
��1��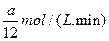
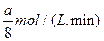
��2��2316
��3��
��4��<
��5��i.���������С����Ӧ���Ũ���������ʹ��Ӧ��������
ii.��С�����С�������ѹǿ����ƽ��������������ٵķ����淴Ӧ�����ƶ������ʹ��Ӧ��ת���ʼ�С
�����������
�����Ѷȣ���
4��ѡ���� �ں��¡����ݵ��ܱ������У��������·�Ӧ��3A��g��+B��g��?XC��g��
��3mol?A��2mol?B����һ�������·�Ӧ���ﵽƽ��ʱC���������Ϊa
����A��B��C��ʼͶ������ʵ����ֱ�Ϊn��A����n��B����n��C��������ͬ�����´ﵽƽ��ʱ��C���������ҲΪa
�����й�������ȷ���ǣ�������
A������ﵽƽ��ʱ��A��B��C������1mol����B��ת����һ������
B������ƽ������ټ���6mol?A��4mol?B�����C�������������a���ɶ϶�X��4
C����X=2������ϵ����ʼ���ʵ���Ӧ���㣺3nB=nA+3
D������ϵ����ʼ���ʵ�������3n��c��+4nA=12nB������ƶϣ�X=4
�ο��𰸣�A����Cת��������ʽ��ߣ��ɵõ� n��A��=4+3x��n��B��=3+1x����x=4����4+3x������3+1x����3��2��Bת���ʽ��ͣ�A��ת��������A����
B������ƽ������ټ���6mol?A��4mol?B����ЧΪ����ѹǿ��������������䣬��x=4ʱ��C���������ӦΪa���ִ���a��˵��ƽ�������ƶ�����x��4����B����
C����X=2ʱ����Ӧǰ��������������仯��ֻҪ��һ�˰������淴Ӧ��ʽ��ȫת��Ϊ��һ�˵����ʺ��Ӧ���ʵ����ʵ�����ȼ��ɣ���n��A��+32n��C��=3��n��B��+12n��C��=2����ʽ��������ã�3n��B��=n��A��+3����C��ȷ��
D�����x=4������ѧ������ת������ߣ�����[n��A��+34n��C��]��[n��B��+14n��C��]=3��2����3n��C��+4n��A��=12nB��
���x��4������ѧ������ת������ߣ�����n��A��=3mol��n��B��=2mol���ɣ���[n��A��+34n��C��]=3��[n��B��+14n��C��]=2���ɵ�3n��C��+4n��A��=12nB����D����
��ѡ��C��
���������
�����Ѷȣ���
5������� ��1���������������������£��о��ı���ʼ�������ʵ�������n��H2����ʾ�ݶ�N2(g)��3H2(g) 2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
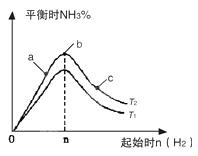
�ٱȽ���a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ���__________��
���������ݻ�Ϊ1L��n��3mol����Ӧ�ﵽƽ��ʱN2��H2��ת���ʾ�Ϊ60%��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ__________mol���������£�T2������Ӧ��ƽ�ⳣ��K��_________�����¶�����ʱ��ƽ�ⳣ����__________��
��ͼ����T2��T1�Ĺ�ϵ��__________��������ڡ��������ڡ��������ڡ�������ȷ��������
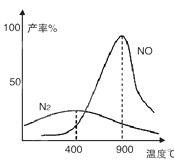
��2��������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�����ͼ����
4NH3��5O2 4NO��6H2O ��4NH3��3O2
4NO��6H2O ��4NH3��3O2 2N2��6H2O
2N2��6H2O
�¶Ƚϵ�ʱ������__________Ϊ�����¶ȸ���900��ʱ��NO�����½���ԭ����___________________
�ο��𰸣���14�֣���1����c?��1��K=25/12��2.08����С�۵���?����2�֣�
��2��N2��������������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½�?����2�֣�
�����������1��������ʱ�¶���ͬ��������Խ������ת����Խ����c���ת������ߣ��ʴ�Ϊ��c��
��N2��g��+3H2��g�� 2NH3��g��
2NH3��g��
��ʼ x? 3? 0
ת��0.6 ?1.8? 1.2
ƽ��x-0.6? 1.2? 1.2
N2��ת����Ϊ60%����
0.6mol/x��100%=60%�����x=1mol��
��Ӧ��ƽ�ⳣ��K=(1.2mol��L��1)2/0.4mol��L��1��(1.2mol��L��1)3=2.08��mol��L��1���D2��
��ͼ��֪���¶ȵͰ����ĺ�����������ӦΪ���ȷ�Ӧ���������¶���ƽ�ⳣ����С��
�ʴ�Ϊ��1��2.08��mol��L��1���D2����С��
����ͼ��֪������������ͬʱ��T1�ȴﵽƽ����ƽ��ʱ������Ũ��С����T2����T1���ʴ�Ϊ�����ڣ�
��2������ͼ���֪�¶ȵ�ʱ���ɵ������¶ȸ�ʱ����NO�����÷�ӦΪ���ȷ�Ӧ�����¶ȸ���900��ʱ��NO�����½����ʴ�Ϊ��N2��������������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½���
�����Ѷȣ�һ��