|
�߿���ѧ֪ʶ���ܽᡶ�������������Ԥ�⣨2019�����°棩(��)
2019-05-30 03:51:14
�� �� �� ��
|
1��ѡ���� ���з�Ӧ�У���ֻ�����ɸۻ��������
A������������ϡHNO3��Ӧ
B����������������Ӧ
C��������������Ӧ
D�����ȵ�������ˮ������Ӧ
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ����
����1 �����Һ�м�����������ۣ���ַ�Ӧ���ˡ�?�����������м������������ᣬ��ַ����ٹ��˼��õ�ͭ��
����1���漰�����������ӵ���������ǿ������˳��Ϊ��_____________________���˲���ʱ����Ҫ�õ��IJ��������ǣ�______________________
����2���ڷ�Һ�м������������������Һ��pH=1����ͭ��ʯī���缫���е�⡣���۲쵽���������������ݲ���ʱ����ֹͣ��⣬��ʱҪ���յ�Cu��ȫ��������
����2��ͭ��______�����������ĵ缫��ӦΪ(���ж���缫��Ӧ���밴�շ�Ӧ�������Ⱥ�˳��ȫ��д��)_______________________________________________________?��һ�缫�������ĵ缫��ӦΪ_____________________________?����2�ڵ缫��ֱ�ӻ���ͭ�������ϱȷ���1��㣬������2Ҳ�в���֮������Ҫ����Ϊ�� ______________________
�ο��𰸣�������1��Fe3��>Cu2��>H��>Fe2��?©�����ձ�������������2����? 2Fe3����2e��=2Fe2����? Cu2����2e��="Cu" ��2H����2e��=H2����? 2Cl����2e��=Cl2������Ⱦ������Cl2����?��ʹ���˵��װ�ã��ɱ��ϸߵȡ�
��������������Է�Һ�л���CuΪ�زģ���������ԭ��Ӧ֪ʶ�͵绯ѧ֪ʶ���ܵĽ������������1��ͬʱ�����˹��˲���������2���õ��ķ�������Cu����ͭ��ʯī���缫��ͭҪ���������������������õ��ӣ�����Һ�к���Fe3����Cu2����H����Fe2�������Դ��ڵõ���˳�����⣬�ɷ���1��֪��������ǿ������˳��ΪFe3��>Cu2��>H��>Fe2�����ʵõ���˳��ΪFe3��>Cu2��>H��>Fe2����������֪Fe3����Cu2����H���ֱ��Ⱥ��������õ��ӡ����һ�ʻ��ӻ����;��÷��濼���˷����IJ��㡣
�����Ѷȣ�һ��
3������� ij��������Ʒ�к���������FeSO4���ʡ�ijͬѧҪ�ⶨ������Ԫ�ص���������������������·������вⶨ����������Ϊ��
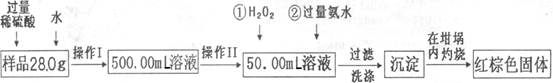
��������̻ش�
��1������I��������Һʱ�����õ��IJ����������ձ�����Ͳ������������ͷ�ι����⣬��������??(���������ƣ���
��2������II�б����õ���������?��
A��50mL��Ͳ
B��100mL��Ͳ
C��50mL��ʽ�ζ���
D��50mL��ʽ�ζ���
| ��3����Ӧ���У���������H2O2��Һ��Ӧ�����ӷ���ʽ?��
��4�����������SO42���Ƿ����Ӹɾ��IJ���?
?��
��5������������ȣ���ȴ�����£�����ƽ������������Ⱥ�����������Ϊblg���ٴμ��Ȳ���ȴ�����³���������Ϊb2g����b1��b2=0.3����Ӧ���еIJ�����?
?��
��6��������������Ϊ42.6g��������������Ⱥ�ͬ���������Ϊ44.8g������Ʒ����Ԫ�ص���������=?(����һλС������
��7����һͬѧ��Ϊ����������ʵ�鲽��̫����������Ϊ��ֻҪ����Ʒ����ˮ���ֽ��裬�����������ճ������ɣ���������������������Ƿ���У�?��������С������С���
�ο��𰸣���16�֣���1��500mL����ƿ��2�֣�?��2��C��2�֣�����
��3��2Fe2++H2O2+2H+=2Fe3++2H2O��3�֣�
��4��ȡ�������һ��ϴ��Һ���Թ��У�����Ba(NO3)2����BaCl2����Һ�����ް�ɫ�����������ϴ����2�֣�
��5���������ȣ���ȴ�����¡�������ֱ�������������������0.1g��2�֣�
��6��55.0%��3�֣�?��7�������У�2�֣�
�����������1����������һ�����ʵ���Ũ����Һ�ķ�����֪������500.00mL��Һ�Ⱥ���Ҫ�ձ�����Ͳ����������500mL����ƿ����ͷ�ιܵ���������2����Ͳ�ľ�ȷ��һ��Ϊ0.1mL���ζ��ܵľ�ȷ��һ��Ϊ0.01mL��Fe2O3+3H2SO4(����)=Fe2(SO4)3+3H2O������������������������Ļ����Һ�����ԣ���ȡ50.00mL������ҺӦ��ѡ��50mL��ʽ�ζ��ܣ���ֻ��C��ȷ����3��˫��ˮ�dz�����ɫ����������Ŀ���ǽ�������������Ϊ�����������ݻ��ϼ��������������������ԭ�Ӹ����غ��֪��2Fe2++H2O2+2H+=2Fe3++2H2O����4��H++NH3?H2O= H2O +NH4+��Fe3++3NH3?H2O=Fe(OH)3��+3NH4+��Fe(OH)3�������������ſ����Ե�����李���ˮ������SO42�D+Ba2+=BaSO4������˳��ÿ����Ա�����Һ����SO42�D�Ƿ�ϴ�Ӹɾ�����5��2Fe(OH)3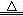 Fe2O3+3H2O����b1��b2������ȣ�˵��Fe(OH)3����������ȫ�ֽ�ΪFe2O3���壬��b1��b2=0.3��˵��Fe(OH)3����û�г��ֽ⣬�����Ҫ��ʢ��Fe(OH)3�������������ж�μ��ȡ��ڸ���������ȴ����������¼������ֱ����������������ȣ���6��������������������m(Fe2O3)=44.8g��42.6g=2.2g��������Ԫ�ص�������Fe2O3=2Fe+3O����m(Fe)= m(Fe2O3)��112/160=��44.8g��42.6g����112/160��������Ԫ�������غ��֪��50.00mL����Һ��m(Fe)=��44.8g��42.6g����112/160����500.00mL����Һ��m(Fe)=��44.8g��42.6g����112/160��500.00mL/50.00mL��������Ԫ�������غ��֪��28.0g��Ʒ��m(Fe)=��44.8g��42.6g����112/160��500.00mL/50.00mL���������Ʒ����Ԫ�ص�����������w(Fe)=" m(Fe)/" m(��Ʒ)��100%=��44.8g��42.6g����112/160��500.00mL/50.00mL��28.0g��100%=55.0%����7����Ʒ��Fe2O3������ˮ��FeSO4������ˮ�������ܴٽ�FeSO4ˮ������Fe(OH)2��H2SO4��Fe(OH)2�ױ�����ΪFe(OH)3��H2SO4�ѻӷ���Fe(OH)3��H2SO4�����кͷ�Ӧ����Fe2(SO4)3��H2O���������ղ���ʹFe2(SO4)3��Һ�ֽ�ΪFe2O3���ʸ÷��������С� Fe2O3+3H2O����b1��b2������ȣ�˵��Fe(OH)3����������ȫ�ֽ�ΪFe2O3���壬��b1��b2=0.3��˵��Fe(OH)3����û�г��ֽ⣬�����Ҫ��ʢ��Fe(OH)3�������������ж�μ��ȡ��ڸ���������ȴ����������¼������ֱ����������������ȣ���6��������������������m(Fe2O3)=44.8g��42.6g=2.2g��������Ԫ�ص�������Fe2O3=2Fe+3O����m(Fe)= m(Fe2O3)��112/160=��44.8g��42.6g����112/160��������Ԫ�������غ��֪��50.00mL����Һ��m(Fe)=��44.8g��42.6g����112/160����500.00mL����Һ��m(Fe)=��44.8g��42.6g����112/160��500.00mL/50.00mL��������Ԫ�������غ��֪��28.0g��Ʒ��m(Fe)=��44.8g��42.6g����112/160��500.00mL/50.00mL���������Ʒ����Ԫ�ص�����������w(Fe)=" m(Fe)/" m(��Ʒ)��100%=��44.8g��42.6g����112/160��500.00mL/50.00mL��28.0g��100%=55.0%����7����Ʒ��Fe2O3������ˮ��FeSO4������ˮ�������ܴٽ�FeSO4ˮ������Fe(OH)2��H2SO4��Fe(OH)2�ױ�����ΪFe(OH)3��H2SO4�ѻӷ���Fe(OH)3��H2SO4�����кͷ�Ӧ����Fe2(SO4)3��H2O���������ղ���ʹFe2(SO4)3��Һ�ֽ�ΪFe2O3���ʸ÷��������С�
�����Ѷȣ�����
4������� (15 ��)��������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷Ͼɵ�ص�ͭñ(Cu��Zn �ܺ���ԼΪ99%)����Cu���Ʊ�ZnO �IJ���ʵ��������£�
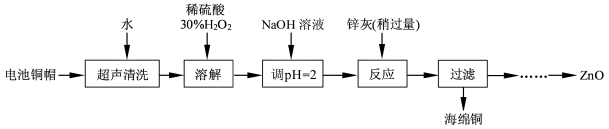
(1)��ͭñ�ܽ�ʱ����H2O2��Ŀ����?(�û�ѧ����ʽ��ʾ)����ͭñ�ܽ���ȫ�� �轫��Һ�й�����H2O2��ȥ����ȥH2O2�ļ�㷽����?��
(2)Ϊȷ������п��(��Ҫ�ɷ�ΪZn��ZnO������Ϊ������������)������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�������ҺpH=3~4�����������KI����Na2S2O3����Һ�ζ����յ㡣���������з�Ӧ�����ӷ���ʽ���£�ҡҡ2Cu2��+4I��=2CuI(��ɫ)��+I2? 2S2O32�� +I2=2I��+S4O62��
�ٵζ�ѡ�õ�ָʾ��Ϊ?���ζ��յ�۲쵽������Ϊ?��
�����ζ�ǰ��Һ�е�H2O2û�г��������ⶨ��Cu2����������?(�ƫ�ߡ�����ƫ�͡����䡱)��
(3)��֪pH>11 ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2-���±��г��˼������������������������pH(��ʼ������pH ����������Ũ��Ϊ1. 0 mol��L-1����)��
?
| ��ʼ������pH
| ������ȫ��pH
| Fe3��
| 1. 1
| 3. 2
| Fe2��
| 5. 8
| 8. 8
| Zn2��
| 5. 9
| 8. 9
|
ʵ���п�ѡ�õ��Լ���30%H2O2��1. 0 mol��L-1HNO3��1. 0 mol��L-1NaOH���ɳ�ȥͭ����Һ�Ʊ�ZnO ��ʵ�鲽������Ϊ����?����?���۹��ˣ���?���ݹ��ˡ�ϴ�ӡ������900�����ա�
�ο��𰸣�(1)��Cu+H2O2+H2SO4=CuSO4+2H2O?�ڼ���(����)
(2)�ٵ�����Һ?��ɫ��ȥ?��ƫ��
(3)������Һ�м�������30% H2O2��ʹ���ַ�Ӧ
�ڵμ�1.0 mol��L-1NaOH��������ҺpH ԼΪ5(��3.2��pH<5.9)��ʹFe3��������ȫ
����Һ�еμ�1. 0 mol��L-1NaOH��������ҺpH ԼΪ10(��8. 9��pH��11)��ʹZn2��������ȫ
�����������1��Ŀ�귴Ӧ������֪��������Ӧ��ӵõ�����Ӧ��Ҳ�ж�Ӧ������ã��÷�Ӧ�����ڸ��ֽ���ε�ˮ�⣬�����ɵ������Ǽ��飻
��2��ϡ������������Ƿ�Ӧ�һ��������������ֹ�����������������ļ��������Ϊԭ��������д洢����ȫ���ų�������������������ᷴӦҲ������������ɼ��������52molH2������Al������ǿ�Ƚϵͣ����������˷�Ӧ������������Ҫ�������������ʡ�
��3�����Ǹ����Dz��ϣ����븺����Ӧ����ʧȥ���Ӳ�����������������ӷ�Ӧ����ƫ��������ӣ������������õ�������������
�����㶨λ���ϵ����ͭ�Ļ��ա�ZnO���Ʊ�ʵ��
�����Ѷȣ�һ��
5��ʵ���� ��6�֣�ij��ѧ��ȤС��������ʯ����Ҫ�ɷ�ΪFe203������Si02��A1203
�����ʣ���ȡFe2O3�������ֳ����£�

��1��(I���ͣ������з�����Һ�ͳ����IJ���������?��
��2������A����Ҫ����?������B��?��
��3����ҺY�е������ӳ�OH-��Cl-�⣬����?��
��4��д��������������Fe(OH)3�����ӷ���ʽ?
�ο��𰸣�(1) ����? (2)SiO2���������? Fe203�������� (3 [Al(OH)4]-��A102-? (4)Fe3++3OH-==Fe(OH)3��
�����������1�����������ڲ����Թ����Һ��֮���һ�ַ��뷽�������Է�����Һ�ͳ����IJ��������ǹ��ˡ�
��2�������������ȷֽ�����������������B����������
��3����������������Ӧ�����������������ͷ�Ӧ�����Գ���A�Ƕ������衣X�к����Ȼ������Ȼ������������ᡣ����������������������������Һ�У�������ҺY�л�����ƫ�����ơ�
��4���Ȼ������������Ʒ�Ӧ���������������Ȼ��ƣ���Ӧ�����ӷ���ʽ��Fe3++3OH-==Fe(OH)3��
�������������л��е����ʳ�ȥ����ô�������ᴿ;�������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��:
1. ���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ��,�������������ʻ������С�
2. �����ᴿ�������״̬���䡣
3. ʵ����̺Ͳ������������С���ѡ������ᴿ����Ӧ��ѭ��������ѧ,�ȼ��ӵ�ԭ��
�����ᴿ������ѡ��˼·�Ǹ��ݷ����ᴿ������ʺ�״̬�����ġ���������:
1. �����ᴿ���ǹ���(�Ӽ����ӷ���) :����(���ա��������ȷֽ�) ,�ܽ�,����(ϴ�ӳ���) ,����,�ᾧ(�ؽᾧ) ,�羫����
2. �����ᴿ����Һ��(�Ӽ����ӷ���) :��Һ,��ȡ,����
3. �����ᴿ���ǽ���:������������
4. �����ᴿ��������:ϴ����
�����Ѷȣ�һ��
|