1、简答题 某无色溶液含有Na+、Ba2+、Cu2+、HCO3-、SO42-、Cl-等离子中的若干种.依次进行下列实验,现象如下:
①取少量溶液于试管之中,滴入几滴紫色石蕊试液后溶液显红色;
②另取少量的原溶液,先加入过量的NaOH溶液,然后再滴加适量的Na2CO3溶液,产生白色沉淀.
请回答下列问题:
(1)原溶液中肯定存在的离子有______;
(2)原溶液中肯定不存在的阳离子有______,
(3)写出②中发生反应的离子方程式:______;______.
参考答案:溶液无色,则一定不存在Cu2+,
①取少量溶液于试管之中,滴入几滴紫色石蕊试液后溶液显红色,说明溶液呈酸性,则一定不存在HCO3-;
②另取少量的原溶液,先加入过量的NaOH溶液,然后再滴加适量的Na2CO3溶液,产生白色沉淀,则由题目提供离子可知一定存在Ba2+,则一定不存在SO42-,由电荷守恒可知一定存在阴离子Cl-,不能确定是否含有Na+,
(1)由以上分析可知一定含有Ba2+、Cl-,故答案为:Ba2+、Cl-;
(2)溶液无色,则一定不存在Cu2+,原溶液中肯定不存在的阳离子有Cu2+,不能确定是否含有Na+,故答案为:Cu2+;
(3)②中加入氢氧化钠,目的是中和酸,反应的离子方程式为H++OH-=H2O,加入碳酸钠,与反应生成碳酸钡沉淀,反应的离子方程式为Ba2++CO32-=BaCO3↓,
故答案为:H++OH-=H2O;Ba2++CO32-=BaCO3↓.
本题解析:
本题难度:一般
2、选择题 某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是? ( )。
A.K+、Na+、HCO3-、NO3-
B.Na+、SO42-、Cl-、S2-
C.NH4+、Mg2+、SO42-、NO3-
D.H+、K+、Cl-、Na+
参考答案:B
本题解析:能溶解Al(OH)3、Al,而不能溶解Fe的溶液只能是强碱溶液,A项中的HCO3-,C项中的NH4+、Mg2+,D项中的H+都不能在强碱溶液中大量共存。
本题难度:一般
3、选择题 某溶液中含有NO、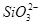 、
、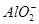 、S2-4种离子,若向其中加入过量的盐酸,微热并搅拌,再加入过量的氢氧化钠溶液,则溶液中离子数目大量减少的是
、S2-4种离子,若向其中加入过量的盐酸,微热并搅拌,再加入过量的氢氧化钠溶液,则溶液中离子数目大量减少的是
A.只有S2-
B.S2-和NO3-
C.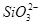 、S2-和NO3-
、S2-和NO3-
D.4种离子都减少
参考答案:B
本题解析:本题通过实验探究4种离子的反应情况,考查离子反应的本质。解答时根据H+、Cl-、Na+、OH-与4种离子的性质,推断出离子数目大量减少的离子。加入过量盐酸,NO3- (H+)氧化S2-,从而导致 NO3-和S2-的数目大量减少,而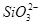 、
、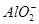 与过量的H+反应生成H2SiO3、Al3+,H2SiO3、Al3+分别与过量的OH-反应又生成
与过量的H+反应生成H2SiO3、Al3+,H2SiO3、Al3+分别与过量的OH-反应又生成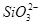 和
和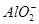 ,数目几乎不变。
,数目几乎不变。
本题难度:一般
4、选择题 化学知识在生活中有重要意义,下列说法不正确的是
A.草木灰(含有K2CO3)水溶液可以用于洗涤油污
B.乙醇、乙酸和甲醛广泛应用于食品加工
C.捕获排放的CO2能降低地球的温室效应
D.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
参考答案:B
本题解析:碳酸钾是强碱弱酸盐,能水解,其溶液呈碱性,能促进油脂的水解,因此草木灰溶液可用于洗涤油污,故A选项正确;甲醛有毒,对人体有害,不能用于食品加工,故B选项错误;二氧化碳是引起温室效应的主要物质,捕获二氧化碳能降低大气中二氧化碳的浓度,降低地球的温室效应,故C选项正确;形成原电池时,锌块作负极(或阳极),因发生氧化反应而被腐蚀,钢铁作正极(或阴极)而被保护,这是牺牲阳极的阴极保护法,故D选项正确。
本题难度:简单
5、选择题 下列各组离子在指定溶液中能大量共存的是
[? ]
①无色溶液中:K+、Cu2+、Na+、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、NO3-、NH4+
④在由水电离出的c(OH-)=10-13mol・L-1的溶液中:Na+、Ba2+、Cl-、I-
⑤能使pH试纸变为蓝色的溶液:Na+、C1-、S2-、ClO-
⑥酸性溶液中:Fe2+、Al3+、NO3-、Cl-
A.①②⑤
B.③⑤⑥
C.②④
D.②④⑥
参考答案:C
本题解析:
本题难度:一般