1、选择题 硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是
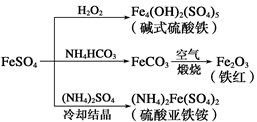
A.制备碱式硫酸铁利用了过氧化氢的氧化性
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质
2、选择题 将a g CuO和b g Fe2O3粉末分别溶于相同体积的足量稀盐酸中,得到CuCl2和FeCl3溶液的物质的量浓度相等(忽略溶液体积的改变)。则a与b的关系为(?)
A.a=2b
B.2a=b
C.a=b
D.无法确定
3、填空题 铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
(1)钢铁的腐蚀
钢铁在潮湿的空气中被腐蚀的负极反应式为:______;将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中,下列叙述正确的是______
A.过一段时间,乙试管中的导管内水柱上升
B.甲试管中铁钉发生了化学腐蚀
C.铁钉在该装置中被腐蚀的情况随时间的延长而加快
(2)生铁中含有一种铁碳化合物X(?Fe3C).?X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是:______;X与过量浓硝酸反应后溶液中含有的盐的化学式______.
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
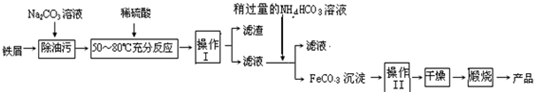
回答下列问题:
①操作Ⅰ的名称是______,操作Ⅱ的名称是______;
②Na2CO3溶液可以除油污,原因是(用离子方程式表示)______;
③请完成生成FeCO3沉淀的离子方程式:Fe2++HCO3-?FeCO3↓+______+H2O;
④写出在空气中煅烧FeCO3的化学方程式______.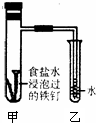
4、简答题 铬铁矿的主要成分可表示为FeO?Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示.

已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O?

?2CrO42-+2H+
请回答:
(1)K2Cr2O7中Cr元素的化合价是?.
(2)生成滤渣1中红褐色物质的反应的化学方程式是?.滤液1的成分除Na2CrO4外,还含有(填化学式)?.
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是?.
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是?.
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、?、过滤、洗涤、干燥.
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是?.
5、推断题 现有甲、乙、丙、丁四种单 质和由其组成元素组成的A、B、C、D四种化合物, 其中甲、乙为非金属气体单质,甲为密度最小的气体,乙能支持燃烧,丙、丁为常见金属,其中丙在地壳中含量处前三位。这些物质间的转化关系如下图所示(反应条件已省略)。

请回答下列问题:
(1)B的俗名___,C物质的用途之一___ 。
(2)写出A+乙B的化学方程式____。
(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为____。
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液Ⅱ(假设各步反应均恰 好进行完全);向溶液I中通入____mol Cl2,经充分反应可恰好使溶质的组成与溶液Ⅱ完全相同。