1、选择题 在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I(aq)。测得不同温度下该反应的平衡常数K如表所示,下列说法正确的是
t/℃
| 5
| 15
| 25
| 35
| 50
|
K
| 1 100
| 841
| 689
| 533
| 409
|
?
A.反应I2(aq)+I-(aq) I(aq)的ΔH>0
I(aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
参考答案:B
本题解析:
由题意知,温度升高,平衡常数减少,则平衡向逆方向移动,正反应为放热反应,A错;其他条件不变,升高温度,平衡向逆方向移动,溶液中c(I3-)减少,B正确;该反应的平衡常数表达式为K= c(I3-)/[ c(I-)c(I2)],C错;平衡常数只与温度有关,加放少量的KI固体对平衡没有影响,D错;答案选B。
本题难度:一般
2、选择题 已知:2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
物质
| CH3OH
| CH3OCH3
| H2O
|
c/(mol・L-1)
| 0.8
| 1.24
| 1.24
|
?
下列说法正确的是(?)
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6 mol/L
③平衡时,反应混合物的总能量减少20 kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08 mol・L-1
A.①②④⑤?B.②⑥? C.②③④⑥?D.②④⑥
参考答案:B
本题解析:因为正反应为放热反应,升高温度平衡常数减小,①错;根据表格数据可知,反应转化生成的CH3OCH3、H2O浓度均为1.24 mol・L-1,此时CH3OH的浓度为0.8 mol・L-1,根据Qc=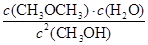 ,将各物质的浓度代入可得,Qc=2.4<400,所以此时没有达到平衡,此时反应向正反应方向进行,⑤错;由化学平衡常数计算可知平衡时c(CH3OCH3)=1.6 mol/L,②对;生成CH3OCH3的物质的量为1.6 mol,根据方程式可知生成1.6 mol×25 kJ・mol-1=40 kJ,③错;平衡时,再加入与起始等量的CH3OH,相当于增大压强,平衡不移动,CH3OH的转化率不变,④错;根据②可知,达到平衡时CH3OH的浓度为0.8 mol・L-1-0.72 mol・L-1=0.08 mol・L-1,⑥对。
,将各物质的浓度代入可得,Qc=2.4<400,所以此时没有达到平衡,此时反应向正反应方向进行,⑤错;由化学平衡常数计算可知平衡时c(CH3OCH3)=1.6 mol/L,②对;生成CH3OCH3的物质的量为1.6 mol,根据方程式可知生成1.6 mol×25 kJ・mol-1=40 kJ,③错;平衡时,再加入与起始等量的CH3OH,相当于增大压强,平衡不移动,CH3OH的转化率不变,④错;根据②可知,达到平衡时CH3OH的浓度为0.8 mol・L-1-0.72 mol・L-1=0.08 mol・L-1,⑥对。
本题难度:一般
3、填空题 一定温度下,将3molA气体和1molB气体通过一密闭容器中,发生如下反应:3A(g)+B(g) xC(g)。
xC(g)。
请填写下列空白:
(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4mol/L。
①1min内,B的平均反应速率为_________;x_________;
②若反应经2min达到平衡,平衡时C的浓度_________0.8mol/L(填“大于”、“等于”或“小于”);
③平衡混合物中,C的体积分数为22%,则A的转化率是_________;
④改变起始物质加入的量,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的关系式_________。
(2)若维持容器压强不变
①达到平衡时C的体积分数_________22%,(填“大于”、“等于”或“小于”);
②改变起始物质加入的量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入_________molA气体和_________molB气体
参考答案:(1)①0.2 mol/(L・min);2;②小于;③36%;④n(A)+3n(C)/2=3、n(B)+ n(C)/2=1
(2)①大于;②6mol;2mol
本题解析:
本题难度:一般
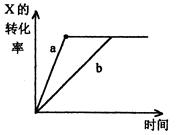
4、选择题 如图,曲线a表示一定条件下,可逆反应X(g) + Y(g)? 2Z(g) +W(s),正反应为放热反应的反应过程,若使a曲线变为b曲线,可采取的措施是

A.减小Y的浓度
B.增大Y的浓度
C.降低温度
D.减小反应体系的压强
参考答案:D
本题解析:由图可知,若使a曲线变为b曲线,反应达到平衡的时间加长,即反应速率降低;平衡时X的转化率不变,则平衡不移动。减小Y的浓度,v降低,平衡左移,A错;增大Y的浓度,v增大,平衡右移,B错;降低温度,v降低,平衡右移,C错;该反应前后气体分子总数相同,减小压强,平衡不移动,速率降低,选D。
点评:化学平衡图像是化学平衡的一个重要知识点,历年高考经常考查,考生在备考过程中应学会分析图像。
本题难度:一般
5、选择题 反应3Fe(s)+4H2O(g)  ?Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
?Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
A.容器内压强不再改变
B.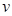 (H2O)=
(H2O)=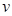 (H2)
(H2)
C.气体的密度不再改变
D.反应不再进行
参考答案:C
本题解析:当变量达到不变时,达到平衡状态,根据方程式可得,反应前气体的系数和和反应后气体的系数相等,气体的物质的量始终不变,故容器内的压强始终不变,当容器内的压强不变时,不能用来判断是否达到了平衡状态,A错误;B、没有指明正反应和逆反应的反应速率相等,故B错误;C、密度等于容器内气体的质量除以容器的体积,水蒸气生成了氢气,气体的质量是个变量,故密度是变量,当密度不变时即达到了平衡状态,故C正确;D、当达到平衡状态时,反应没有停止,只是正反应和逆反应反应速率相等了,故D错误;故选C。
本题难度:一般